摘要: 在 ① H2.② NaCl.③ H2O.④ Na2O2.⑤ H2O2.⑥ NH4Cl.⑦ CO2.⑧ NH4NO3. ⑨ Na2O.⑩ HCl这些物质中.只含有离子键的是 只含有共价键的是 .既含有离子键又含有共价键的是 .属于离子化合物的是 .属于共价化合物的是 .
网址:http://m.1010jiajiao.com/timu3_id_302160[举报]
 (2010?桂林二模)某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).
(2010?桂林二模)某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).(1)该小组同学用该装置进行“H2的制取及燃烧性质验证”实验.他们设计了如下的实验步骤:
a.组装装置并检验气密性
b.装入药品,关闭活塞m和n,固定在铁架台上
c.打开分液漏斗活塞m,使反应开始
d.当观察到B中有较多气体时,打开活塞n并点燃气体
回答下列问题:
①以上某步骤中有一处明显的操作错误,请指出错误之处
d步骤中在点燃H2前没有先验纯.
d步骤中在点燃H2前没有先验纯.
②该小组同学在进行c步骤操作时,发现分液漏斗中的溶液不能滴下,你认为可能的原因有
一是分液漏斗的玻璃塞没有打开,二是量气管中液面高于分液漏斗中液面.
一是分液漏斗的玻璃塞没有打开,二是量气管中液面高于分液漏斗中液面.
.(2)该装置还可用于制取并收集少量其他气体,用字母代号填空:下列气体中哪些可以用该装置来制取和收集
A、B、E
A、B、E
;若将装置B中的水换成CCl4,下列气体中哪些可以用该装置来制取和收集A、B、C、D
A、B、C、D
.A.O2 B.NO C.SO2 D.NH3 E.C2H2 F.C2H4
(3)该小组同学用该装置进行定量实验,以确定某稳定饱和脂肪醇的结构.
①反应前,先对量气管进行第一次读数,读数为40.0mL,然后在A中加入5gNa和0.62g待测醇,充分反应后,再进行第二次读数,读数为264.0mL(所有数据均已换算成标准状况时的数值).读数时要注意的是:一是使视线与凹液面最低处相平,二是
保持装置A和装置B液面相平
保持装置A和装置B液面相平
.②为了进一步确定该醇的结构,又将0.62g该醇充分燃烧,可以生成0.02mol的CO2和0.03mol的H2O,已知两个或者两个以上的羟基连在同一个C原子上不能形成稳定的醇,根据上述信息计算确定该饱和醇的结构简式为
CH2OHCH2OH
CH2OHCH2OH
. (2012?汕头二模)甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.
(2012?汕头二模)甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.(1)工业生产甲醇的常用方法是:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ/mol.
已知:2H2(g)+O2(g)=2H2O (l)△H=-571.6kJ/mol
H2(g)+
| 1 |
| 2 |
①H2的燃烧热为
285.8
285.8
kJ/mol.②CH3OH(g)+O2(g)?CO(g)+2H2O(g)的反应热△H=
-392.8KJ/mol
-392.8KJ/mol
.③若在恒温恒容的容器内进行反应CO(g)+2H2(g)?CH3OH(g),则可用来判断该反应达到平衡状态的标志有
AD
AD
.(填字母)A.CO百分含量保持不变
B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变
D.CO的生成速率与CH3OH的生成速率相等
(2)工业上利用甲醇制备氢气的常用方法有两种:
①甲醇蒸汽重整法.该法中的一个主要反应为CH3OH(g)?CO(g)+2H2(g),此反应能自发进行的原因是
该反应是一个熵增的反应
该反应是一个熵增的反应
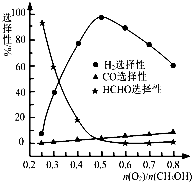
.②甲醇部分氧化法.在一定温度下以Ag/CeO2-ZnO为催化剂时原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如图所示.则当n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应方程式为
2CH3OH+O2
2HCHO+2H2O
| 催化剂 |
| 加热 |
2CH3OH+O2
2HCHO+2H2O
;在制备H2时最好控制n(O2)/n(CH3OH)=| 催化剂 |
| 加热 |
0.5
0.5
.(3)在稀硫酸介质中,甲醇燃料电池负极发生的电极反应式为
CH3OH-6e-+H2O=CO2↑+6H+
CH3OH-6e-+H2O=CO2↑+6H+
.化学试验中必须注意安全,以下实验操作或事故处理中正确的是( )
①在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中并不断用玻璃棒搅拌
③浓碱液对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液
④给试管中的液体加热时,液体应不超过试管容积的
⑤点燃装满酒精的酒精灯.
①在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中并不断用玻璃棒搅拌
③浓碱液对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液
④给试管中的液体加热时,液体应不超过试管容积的
| 1 |
| 3 |
⑤点燃装满酒精的酒精灯.
查看习题详情和答案>>
氨在国民经济中占有重要的地位,请参与下列探究.
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气.C(s)+H2O(g)?H2(g)+CO(g)△H=+131.3kJ/mol,△S=+133.7J/K
该反应在低温下能否自发 (填:能或否).
(2)已知在400℃时,N2 (g)+3H2(g)?2NH3(g)△H<0 的K1=0.5,
①2NH3(g)?N2 (g)+3H2(g)的K2= (填数值).
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正 V(N2)逆(填:>、<、=、不能确定).
(3)已知反应:CO(g)+2H2(g)?CH3OH (g)△H<0
a.该反应在一定条件下达到平衡后,在保证H2浓度不变的情况下,增大容器的体积,试根据平衡常数,判断平衡
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
b.若该反应的逆反应速率与时间的关系如图所示:
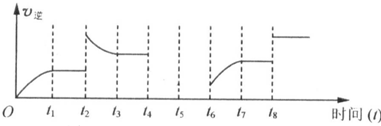
t2时的平衡常数K与t1时的相比可能 (填字母代号)
A.增大 B.减小 C.不变.
查看习题详情和答案>>
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气.C(s)+H2O(g)?H2(g)+CO(g)△H=+131.3kJ/mol,△S=+133.7J/K
该反应在低温下能否自发
(2)已知在400℃时,N2 (g)+3H2(g)?2NH3(g)△H<0 的K1=0.5,
①2NH3(g)?N2 (g)+3H2(g)的K2=
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正
(3)已知反应:CO(g)+2H2(g)?CH3OH (g)△H<0
a.该反应在一定条件下达到平衡后,在保证H2浓度不变的情况下,增大容器的体积,试根据平衡常数,判断平衡
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
b.若该反应的逆反应速率与时间的关系如图所示:

t2时的平衡常数K与t1时的相比可能
A.增大 B.减小 C.不变.