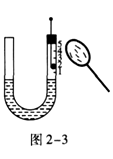
摘要:27.实验小组用如图2-8所示的装置进行实验. 图2-8 (1)根据实验.回答问题. 表2-6 实验步骤 简答 第一步,称取3g高锰酸钾与少量二氧化锰混合后放入装置①的试管中.点燃酒精灯 装置①的试管中发生反应的文字表达式: 第二步:加热试管一段时间后.用橡皮管连接a.b 刚开始加热时.排出的气体不宜立即收集.原因是: 第三步:当装置②中水面不再下降.断开a.b.移去酒精灯.将装置②中的集气瓶密封.并贴上标签备用 第四步:读取量筒里水的体积数并记录 读数时.视线必须与液体凹液面的 保持水平 (2)在理解上述实验的基础上.请你归纳本实验的目的: .(3)该实验能否达到目的?为什么? 答案:(1)高锰酸钾锰酸钾+二氧化锰+氧气 刚开始产生的气体中含有空气.不纯净 最低处 (2)测定3g高锰酸钾加热分解产生氧气的体积 (3)不能达到目的.因为在第二步中先加热一段时间.后连接橡皮管会使部分氧气逸散到空气中.所以测得的结果不准确. 知识积累
网址:http://m.1010jiajiao.com/timu3_id_29085[举报]
 实验小组用如图所示的装置进行实验.
实验小组用如图所示的装置进行实验.(1)根据实验,填表回答问题
| 实验步骤 | 简答 | ||||||||
| 第一步;称取3g氯酸钾与少量二氧化锰混合后放入装置①的试管中,点燃酒精灯 | 装置①的试管中发生反应的符号表达式: 2KClO3
2KClO3
| ||||||||
| 第二步:加热试管一段时间后,用橡皮管连接a、b | 刚开始加热时,排出的气体不宜立即收集,原因是: 这时排出的是试管中的空气 这时排出的是试管中的空气 | ||||||||
| 第三步:当装置②中水面不再下降,断开a、b,移去酒精灯,将装置②中的集气瓶密封,并贴上标签备用 | |||||||||
| 第四步:读取量筒里水的体积数并记录 | 读数时,视线必须与液体凹液面的 最低处 最低处 保持水平 |
制取氧气并测量氧气体积
制取氧气并测量氧气体积
.(3)该实验能否达到目的?为什么?
能,利用产生的氧气形成气压把水排进量筒内;
能,利用产生的氧气形成气压把水排进量筒内;
.金属材料在国防建设中起着重要的作用,图1为歼-15飞机在辽宁舰上起飞.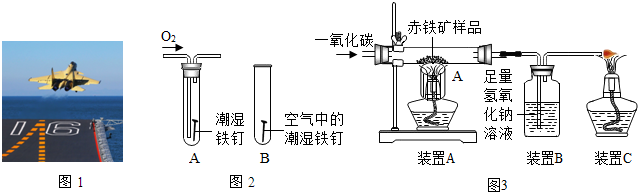
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 .
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁锈蚀主是铁与空气中的 共同作用的结果,为了避免轮船钢质外壳被腐蚀,通常用 方法防锈.
(3)某小组用如图2所示装置对铁生锈的条件进行探究.一段时间后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是 .
(4)工业生产常用10%的稀盐酸来除铁锈,写出除锈的化学方程式 .实验室用浓盐酸配制10%的稀盐酸时,用到的主要仪器有 .
(5)用如图3所示的装炼铁,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称量赤铁矿样品的质量为wg).
①实验过程中的主要步骤有:a检验CO的纯度,通入一氧化碳;b装入药品并固定;c加热;d停止加热.其中正确的实验步骤是 .
②装置A中发生反应的方程式为 ;装置C的作用是 .
③要测定赤铁矿样品中氧化铁的质量分数,需要测量的数据是 .(填一种答案即可)
查看习题详情和答案>>

(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁锈蚀主是铁与空气中的
(3)某小组用如图2所示装置对铁生锈的条件进行探究.一段时间后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是
(4)工业生产常用10%的稀盐酸来除铁锈,写出除锈的化学方程式
(5)用如图3所示的装炼铁,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称量赤铁矿样品的质量为wg).
①实验过程中的主要步骤有:a检验CO的纯度,通入一氧化碳;b装入药品并固定;c加热;d停止加热.其中正确的实验步骤是
②装置A中发生反应的方程式为
③要测定赤铁矿样品中氧化铁的质量分数,需要测量的数据是
 25、日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.
25、日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.(1)根据以上信息,请你总结出ClO2的物理性质
①②③
(填序号);(2)目前欧洲一些国家采用氯酸钠(NaClO3)与浓盐酸反应制取ClO2(Kestiog法),反应的化学方程式为:2NaClO3+4HCl=2ClO2+Cl2↑+2H2O+2NaCl.我国最近研究成功用氯气和亚氯酸钠(NaClO2)反应制取ClO2,该反应的化学方程式为Cl2+2NaClO3=2ClO2+2NaCl,此法与Kestiog法相比,其优点是
反应后没有Cl2生成,便于分离,不污染环境
.(3)某实验小组用如图所示装置探究用潮湿的KClO3与草酸在60℃时反应制取ClO2获得成功.在装置中:A为ClO2的发生装置,B为ClO2收集装置,C为尾气吸收装置.请分析回答:
①为了收集到液态ClO2,对装置B应采取的措施是
用冰冷却
.②为较好地防止ClO2泄漏,C的烧杯中应盛放的液体是
氢氧化钠溶液(或碱溶液)
.
日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.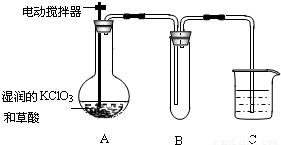
(1)根据以上信息,请你总结出ClO2的物理性质______(填序号);
(2)目前欧洲一些国家采用氯酸钠(NaClO3)与浓盐酸反应制取ClO2(Kestiog法),反应的化学方程式为:2NaClO3+4HCl=2ClO2+Cl2↑+2H2O+2NaCl.我国最近研究成功用氯气和亚氯酸钠(NaClO2)反应制取ClO2,该反应的化学方程式为Cl2+2NaClO3=2ClO2+2NaCl,此法与Kestiog法相比,其优点是______.
(3)某实验小组用如图所示装置探究用潮湿的KClO3与草酸在60℃时反应制取ClO2获得成功.在装置中:A为ClO2的发生装置,B为ClO2收集装置,C为尾气吸收装置.请分析回答:
①为了收集到液态ClO2,对装置B应采取的措施是______.
②为较好地防止ClO2泄漏,C的烧杯中应盛放的液体是______.
查看习题详情和答案>>

(1)根据以上信息,请你总结出ClO2的物理性质______(填序号);
(2)目前欧洲一些国家采用氯酸钠(NaClO3)与浓盐酸反应制取ClO2(Kestiog法),反应的化学方程式为:2NaClO3+4HCl=2ClO2+Cl2↑+2H2O+2NaCl.我国最近研究成功用氯气和亚氯酸钠(NaClO2)反应制取ClO2,该反应的化学方程式为Cl2+2NaClO3=2ClO2+2NaCl,此法与Kestiog法相比,其优点是______.
(3)某实验小组用如图所示装置探究用潮湿的KClO3与草酸在60℃时反应制取ClO2获得成功.在装置中:A为ClO2的发生装置,B为ClO2收集装置,C为尾气吸收装置.请分析回答:
①为了收集到液态ClO2,对装置B应采取的措施是______.
②为较好地防止ClO2泄漏,C的烧杯中应盛放的液体是______.
查看习题详情和答案>>