摘要:33.将4.6g Na溶于95.6g水配成溶液.其密度为1.10 g·mL-1.求: (1)该溶液中NaOH的质量分数为 . (2)该溶液中NaOH的物质的量浓度为 .
网址:http://m.1010jiajiao.com/timu3_id_284704[举报]
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用.
完成下列计算:
(1)将4.6g金属钠投入100克水中,充分反应.已知:2Na+2H2O→2NaOH+H2↑
①生成标准状况下氢气 L.
②求反应后溶液中NaOH的质量分数 %.(两位小数)
(2)将10g CO和CO2的混合气体,通过装有足量过氧化钠的干燥管,反应后干燥管的总质量增加了5.6g.
已知:2Na2O2+2CO2→2Na2CO3+O2,求原混合气体中CO2的质量分数.计算过程: .
(3)NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:
Na2CO3+nH2O→Na2CO3?nH2O(n为平均值,n≤10).
取没有妥善保管已部分变质的NaHCO3样品A 9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表.(不计溶于水的CO2气体)
已知:碳酸钠溶液中逐滴滴入稀盐酸时,反应分两步进行:
Na2CO3+HCl→NaHCO3+NaCl NaHCO3+HCl→NaCl+CO2↑+H2O
试求:
①滴入稀盐酸的物质的量浓度为: .
②当加入盐酸后,生成CO2体积不再增加时,x的最小值为 .
③部分变质后样品A中:NaHCO3的物质的量;Na2CO3?nH2O的物质的量以及n值.计算过程: .
查看习题详情和答案>>
完成下列计算:
(1)将4.6g金属钠投入100克水中,充分反应.已知:2Na+2H2O→2NaOH+H2↑
①生成标准状况下氢气
②求反应后溶液中NaOH的质量分数
(2)将10g CO和CO2的混合气体,通过装有足量过氧化钠的干燥管,反应后干燥管的总质量增加了5.6g.
已知:2Na2O2+2CO2→2Na2CO3+O2,求原混合气体中CO2的质量分数.计算过程:
(3)NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:
Na2CO3+nH2O→Na2CO3?nH2O(n为平均值,n≤10).
取没有妥善保管已部分变质的NaHCO3样品A 9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表.(不计溶于水的CO2气体)
| 盐酸体积(mL) | 8 | 15 | 20 | 50 | x | 120 | 150 |
| 生成CO2体积(mL) | 0 | 112 | 224 | 896 | 2240 | 2240 | 2240 |
Na2CO3+HCl→NaHCO3+NaCl NaHCO3+HCl→NaCl+CO2↑+H2O
试求:
①滴入稀盐酸的物质的量浓度为:
②当加入盐酸后,生成CO2体积不再增加时,x的最小值为
③部分变质后样品A中:NaHCO3的物质的量;Na2CO3?nH2O的物质的量以及n值.计算过程:
三星堆遗址考古的重大发现,揭开了川西平原早期蜀国的面纱,将蜀国的历史推前了两千多年,填补了中国考古学、青铜文化、青铜艺术史上的诸多空白.而硫酸铜是湿法冶金应用极早的一种化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示)

(1)图1烧瓶中发生反应的离子方程式为______;
(2)图2是图1的改进装置,其优点有______;
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在①坩埚中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO4或Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用.[已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为:3.7、6.4.]请回答下列问题:
①方案2中甲物质是______(填字母序号). a.CaO b.CuCO3 c.CaCO3
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45mL 1.5mol?L-1的稀硫酸中,控温在50℃.加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得到CuSO4?5H2O的质量为10.6g.
请回答下列问题:
②加热时温度不宜过高的原因是______,根据有关数据计算出制取CuSO4?5H2O的产率(实际产量与理论产量的百分比)=______.
查看习题详情和答案>>

(1)图1烧瓶中发生反应的离子方程式为______;
(2)图2是图1的改进装置,其优点有______;
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在①坩埚中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO4或Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用.[已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为:3.7、6.4.]请回答下列问题:
①方案2中甲物质是______(填字母序号). a.CaO b.CuCO3 c.CaCO3
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45mL 1.5mol?L-1的稀硫酸中,控温在50℃.加入18mL 10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得到CuSO4?5H2O的质量为10.6g.
请回答下列问题:
②加热时温度不宜过高的原因是______,根据有关数据计算出制取CuSO4?5H2O的产率(实际产量与理论产量的百分比)=______.
(8分)现将25.6g Cu投入50mL 12mol/L的浓硝酸中,充分反应后,收集到4.48L(标准状态)NO和NO2的混合气体。
(1)被还原硝酸的物质的量是多少?
(2)判断25 6gCu和50mLl2mol/L的硝酸反应后何者有剩余?其物质的量是多少?
(3)如果往反应后的体系内再加入200Ml 4mol/L的稀硫酸,是否会有气体逸出,写出离子反应方程式,并计算气体的体积(标准状态)。
查看习题详情和答案>>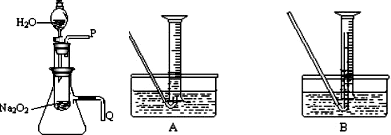 (2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一:有氧气生成;第二:
该反应是放热反应
该反应是放热反应
.Na2O2跟水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(2)某研究性学习小组拟用右图所示装置(气密性良好)
进行实验,以证明上述结论.
用以验证第一条结论的实验操作是:
打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成
打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成
;用以验证第二条结论的实验方法是:
将导管Q浸入水中,反应过程中导管口有气泡冒出
将导管Q浸入水中,反应过程中导管口有气泡冒出
.(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性.请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:
MnO2
MnO2
;现象:气泡迅速产生,能使带火星的木条复燃
气泡迅速产生,能使带火星的木条复燃
.(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论.
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)
B
B
(填序号),理由是防止气体冷却时发生倒吸现象
防止气体冷却时发生倒吸现象
.②若在标准状况下测量气体的体积,应选用的量筒的大小规格为
500mL
500mL
(选填“100mL”“200mL”“500mL”或“1000mL”).(2011?百色模拟)印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
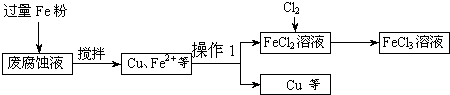
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为
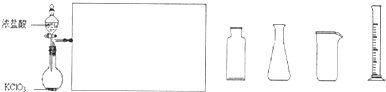
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置.
从图中挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明容器中所装试剂.
(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收.控制生成氯气速率的操作是:
(5)按上述流程操作,需称取Fe粉的质量应不少于
查看习题详情和答案>>

回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是
HCl
HCl
(填化学式).(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为
KClO3+6HCl
KCl+3Cl2↑+3H2O
| ||
KClO3+6HCl
KCl+3Cl2↑+3H2O
.
| ||
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置.
从图中挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明容器中所装试剂.

(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收.控制生成氯气速率的操作是:
缓慢旋转分液漏斗的活塞,调节浓盐酸滴下的速度
缓慢旋转分液漏斗的活塞,调节浓盐酸滴下的速度
.(5)按上述流程操作,需称取Fe粉的质量应不少于
39.2
39.2
g(精确到0.1g),需通入Cl2的物质的量不少于0.75
0.75
mol,加入烧瓶中的KClO3的质量应不少于30.6
30.6
g(精确到0.1g).