摘要:4.实验室制取下列气体时.与实验室制氨气的气体发生装置相同的是: A.O B.Cl C.H D.CO 5在N02与水的反应中.N02作为: A.只作还原剂 B.只是氧化剂 C.既是氧化剂又是还原剂D.既不是氧化剂.又不是还原剂 6 在,下列过程中.需要加快反应速率的是: A.食物腐败 R钢铁腐蚀 C.炼钢 U.D塑料老化 7,X-一反应物的浓度是1.Omol/L.经过20s后.它的浓度变成0,2mol/L.在这20s内. 它的反应速率为: A.0.04 B.0.8mol/(L·S1 C.0.04mol/D.0.04nmt/k. 8在一定条付下.使NO和02在一密闭容器中进行反应.下列蜕法中不m偷的是’ A.反应开始时.正反应速率最大.逆反应速率为零 B.随着反应的进行.正反应速率逐渐减小.最后为零 C.随着反应的进行.逆反应速率逐渐增大.最后不变 D.随着反应的进行.正反应速率逐渐减小.最后不变
网址:http://m.1010jiajiao.com/timu3_id_279057[举报]
|
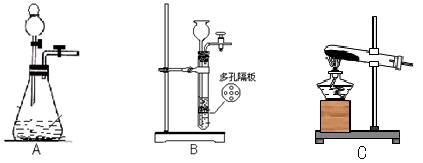
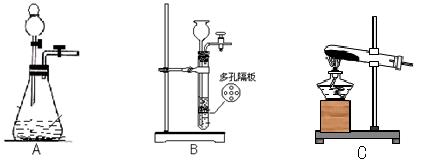
(1)若实验室选用装置C制取氨气,则反应的化学方程式为
________________________________________
 ______________________,
______________________,检验NH3收
 满的方法:____________________________________________________;
满的方法:____________________________________________________;(2)若实验室利用过氧化钠与水反应制取氧气,则应选择__________装置,有关反应的化学方程式为:________________________________________________。 查看习题详情和答案>>
|
(1)若实验室选用装置C制取氨气,则反应的化学方程式为
________________________________________
 ______________________,
______________________,检验NH3收
 满的方法:____________________________________________________;
满的方法:____________________________________________________;(2)若实验室利用过氧化钠与水反应制取氧气,则应选择__________装置,有关反应的化学方程式为:________________________________________________。
实验室可以通过以下三条途径按不同要求制取氮气:
①加热NaNO2(一种致癌物质,有毒)与NH4Cl的混合物浓溶液制取N2;
②将空气通过灼热的活性铜粉制得较纯净的N2;
③加热条件下用NH3还原CuO得纯净的N2和活性铜粉.
如图所示,给出了按上述途径制取N2可供选择的几种实验装置:

请回答下列问题:
(1)按途径①制取N2时,应选用上述装置中的
(2)若只需较纯净的N2,有同学建议把②和③两条途径协同使用,这样做的好处是
(3)按途径③制取N2时,若气流从左到右的顺序所需的上述装置是:A→C→B→D.在A装置中所需要的试剂是
①甲同学:为通过实验现象验证C处有水产生,必须在C装置前后都连接E装置,其中填充的固体药品按前后顺序分别为
②乙同学:实验过程中,发现黑色固体完全变红,质疑此时红色固体可能含Cu2O.通过查阅资料知:Cu2O+2H+=Cu2++Cu+H2O.依据信息,请设计实验证明C处的红色固体中是否含有Cu2O:
③丙同学:实验时充分加热,至C装置硬质玻管质量不再减轻为止.实验完毕后,若实验测得收集的N2体积为aL(已折算为标准状况),硬质玻管质量减轻了bg.则氨分子中氮、氢的原子个数比为(用含a、b的字母的代数式表示)
(此空记3分).
(4)目前工业上用氮气和氢气直接合成氨,氨经一系列反应可制得硝酸.在以上各步反应中,按要求完成化学反应方程式:
①氮元素只发生还原反应
②氮元素既发生氧化反应又发生还原反应:
查看习题详情和答案>>
①加热NaNO2(一种致癌物质,有毒)与NH4Cl的混合物浓溶液制取N2;
②将空气通过灼热的活性铜粉制得较纯净的N2;
③加热条件下用NH3还原CuO得纯净的N2和活性铜粉.
如图所示,给出了按上述途径制取N2可供选择的几种实验装置:

请回答下列问题:
(1)按途径①制取N2时,应选用上述装置中的
F
F
(填装置代码)做发生装置.(2)若只需较纯净的N2,有同学建议把②和③两条途径协同使用,这样做的好处是
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
.(3)按途径③制取N2时,若气流从左到右的顺序所需的上述装置是:A→C→B→D.在A装置中所需要的试剂是
浓氨水
浓氨水
和生石灰
生石灰
.(写试剂名称)①甲同学:为通过实验现象验证C处有水产生,必须在C装置前后都连接E装置,其中填充的固体药品按前后顺序分别为
碱石灰(或无水氯化钙)
碱石灰(或无水氯化钙)
、无水硫酸铜
无水硫酸铜
.(写试剂名称)②乙同学:实验过程中,发现黑色固体完全变红,质疑此时红色固体可能含Cu2O.通过查阅资料知:Cu2O+2H+=Cu2++Cu+H2O.依据信息,请设计实验证明C处的红色固体中是否含有Cu2O:
取样加入稀硫酸后溶液呈蓝色,即证明含Cu2O
取样加入稀硫酸后溶液呈蓝色,即证明含Cu2O
③丙同学:实验时充分加热,至C装置硬质玻管质量不再减轻为止.实验完毕后,若实验测得收集的N2体积为aL(已折算为标准状况),硬质玻管质量减轻了bg.则氨分子中氮、氢的原子个数比为(用含a、b的字母的代数式表示)
| 16a |
| 22.4b |
| 16a |
| 22.4b |
(4)目前工业上用氮气和氢气直接合成氨,氨经一系列反应可制得硝酸.在以上各步反应中,按要求完成化学反应方程式:
①氮元素只发生还原反应
N2+3H2
2NH3
| 高温高压 |
| 催化剂 |
N2+3H2
2NH3
、| 高温高压 |
| 催化剂 |
②氮元素既发生氧化反应又发生还原反应:
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.实验室可以通过三条途径来制取氮气:
①加热条件下用NH3还原CuO制得纯净的N2和活性铜粉,反应的化学方程式为:
![]()
② 将空气通过灼热的活性铜粉制得较纯净的N2
③ 加热NaNO2(有毒性)与NH4Cl的混合浓溶液制取N2,反应的化学方程式为:
![]()
按上述途径制N2可供选择的实验仪器如下图所示,其他必要的仪器如铁架台、铁夹、铁圈、石棉网、酒精灯等未列出。

(l)按途径 ① 制取N2时所需的氨气要用浓氨水与生石灰作原料制取,化学方程式为:
![]() ,最好要用上述仪器中 的(填仪器字母,下同)作为氨气发生装置。要制取并收集纯净的N2(允许含少量的水蒸气),还应使用到上述仪器中的
,最好要用上述仪器中 的(填仪器字母,下同)作为氨气发生装置。要制取并收集纯净的N2(允许含少量的水蒸气),还应使用到上述仪器中的
(2) ① 和 ② 两种途径常常被协同使用。这种方法与途径 ③ 相比优点是
(3)检查 E 装置气密性的方法是 。利用 E 装置还可以制取的气体有 (写出三种)。
查看习题详情和答案>>