摘要: ⑴下面是s能级和p能级的原子轨道图.试回答问题: s电子的原子轨道呈 形.每个s能级有 个原子轨道,p电子的原子轨道呈 形.每个p能级有 个原子轨道. ⑵s电子原子轨道.p电子原子轨道的半径与 因素有关. 具体关系是 . ⑶某元素的原子获得能量后的电子排布式为1s2 2s22p6 3s23p3 4s1.则该元素的原子获得能量前的电子排布式为 ,元素符号为 ,其最高价氧化物对应的水化物的化学式是 .
网址:http://m.1010jiajiao.com/timu3_id_266909[举报]
下面是s能级和p能级的原子轨道图,试回答问题:


s电子的原子轨道呈________形,每个s能级有________个原子轨道;p电子的原子轨道呈________形,每个p能级有________个原子轨道.
(12分)化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一层电子总数,且X和Y具有相同的电子层数;Z与X在周期表中位于同一主族。回答下列问题:K^S*5U.C#O
(1)Y的价电子轨道表示式为 ;
(2)YX2的电子式是 ,分子构型为 ,中心原子发生了____杂化。
(3)Y与Z形成的化合物的分子式是_______,该化合物中化学键是________键(填“极性”或“非极性”),该分子属于__________分子(填“极性”或“非极性”)。[来源:Z*xx*k.Com]
(4)Y的氢化物中分子构型为正四面体的是__ _____(填名称),键角为_______,中心原子的杂化形式为_______。
(5)元素X与Y的电负性的大小关系是___________(用元素符号填写,并填﹥、﹤、﹦),
X与Z的第一电离能的大小关系是___________。(用元素符号填写,并填﹥、﹤、﹦)
(2013?江西二模)(化学-选修物质结构与性质)
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2 np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子.请回答下列问题:
(1)当n=2时,AB2属于
(2)当n=3时,A与B形成的晶体属于
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是
(4)已知某红紫色配合物的组成为CoCl3?5NH3?H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
查看习题详情和答案>>
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2 np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子.请回答下列问题:
(1)当n=2时,AB2属于
非极性
非极性
分子(填“极性”或“非极性”),分子中有2
2
个δ键、2
2
个π键. A6H6分子中A原子的杂化轨道类型是sp2
sp2
杂化.(2)当n=3时,A与B形成的晶体属于
原子
原子
晶体.(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是
S>P>Si
S>P>Si
(用元素符号表示);A、C、D三种元素的第一电离能由大到小的顺序是P>S>Si
P>S>Si
(用元素符号表示).(4)已知某红紫色配合物的组成为CoCl3?5NH3?H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为
1s22s22p63s23p63d6或[Ar]3d6
1s22s22p63s23p63d6或[Ar]3d6
,作为配位体之一的NH3分子的空间构型为三角锥形(或四面体形)
三角锥形(或四面体形)
.(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
1:2
1:2
.
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
(1)A的基态原子最外层有 种不同运动状态的电子,F位于 区。
(2)E2+的基态核外电子排布式为 ,AD4为 (填极性或非极性)分子。
(3)A、B、C三种元素的电负性由小到大的顺序是 (用元素符号表示),B和C两元素中,B的第一电离能较大的原因是 ,与AC2互为等电子体的分子的名称为 。(只写一种)
(4)BD3 中心原子的杂化方式为 ,其分子空间构型为 。
(5)用晶体的x射线衍射法对F的测定得到以下结果:F的晶胞为面心立方最密堆积(如图),又知该晶体的密度为ρg/cm3,晶胞中该原子的配位数为 ;F的原子半径是 pm;(阿伏加德罗常数为NA)。
| A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B元素原子的核外p电子总数比s电子总数少1 |
| C原子p轨道上成对电子数等于未成对电子数,且与A同周期 |
| D元素的族序数与周期数的差为4,且不与A元素在同一周期 |
| E位于周期表中第七列 |
| F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
(2)E2+的基态核外电子排布式为 ,AD4为 (填极性或非极性)分子。
(3)A、B、C三种元素的电负性由小到大的顺序是 (用元素符号表示),B和C两元素中,B的第一电离能较大的原因是 ,与AC2互为等电子体的分子的名称为 。(只写一种)
(4)BD3 中心原子的杂化方式为 ,其分子空间构型为 。
(5)用晶体的x射线衍射法对F的测定得到以下结果:F的晶胞为面心立方最密堆积(如图),又知该晶体的密度为ρg/cm3,晶胞中该原子的配位数为 ;F的原子半径是 pm;(阿伏加德罗常数为NA)。

 已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题:
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题:(1)X、Y、Z第一电离能由小到大的顺序为
(2)E元素基态原子的电子排布式为
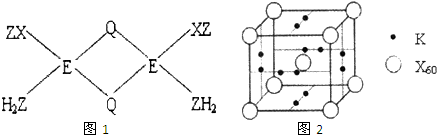
(3)X和Z形成有毒气体XZ,实验室常用EQ溶液吸收并定量测定XZ的含量.反应时,XZ与EQ形成配合物的分子中原子问成键关系如图1所示:E+和Q之间的化学键类型是
(4)XZ2分子中含有
(5)Z氢化物的沸点比Q氢化物的沸点高,理由是
(6)X元素可形成X60.单质,它与金属钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),该化合物中X60与钾原子个数比为