网址:http://m.1010jiajiao.com/timu3_id_228906[举报]
2007年8月《地球学报》杂志报道,利用氮、氧及氮、硼同位素技术,通过测定可知地下硝酸盐来源的水污染情况。完成下列填空:
(1)关于14N与15N的正确说法是 ;
a、自然界氮元素中14N的含量:空气中大于地壳中 b、单质:14N2与15N2互为同位素
c、电子层结构:14N与15N完全相同 d、原子半径:14N小于15N
与N元素同周期且最外层有2个未成对电子的元素相互组成的化合物属于 分子。(填:“极性”、“非极性”、“极性或非极性”)
(2)NH3与H2O分别能与H+ 结合成NH4+与H3O+。与NH4+具有相同空间构型的微粒是 ;
a、H3O+ b、CH4 c、P4 d、NH3
分子中的键角:CH4 P4(填:“>”、“=”或“< ”)。
(3)H3O+ 与NH4+ 的水溶液均显酸性。用离子方程式表示NH4+ 水溶液显酸性的原因:
。
(4)使用N、O、 B同位素,并结合水化学分析,将更有利于对测定结果的解释。写出B原子的最外层电子排布式 ;B原子核外的电子处在 个不同的能级上。
查看习题详情和答案>>
2007年8月《地球学报》杂志报道,利用氮、氧及氮、硼同位素技术,通过测定可知地下硝酸盐来源的水污染情况。完成下列填空:
(1)关于14N与15N的正确说法是 ;
a、自然界氮元素中14N的含量:空气中大于地壳中 b、单质:14N2与15N2互为同位素
c、电子层结构:14N与15N完全相同 d、原子半径:14N小于15N
与N元素同周期且最外层有2个未成对电子的元素相互组成的化合物属于 分子。(填:“极性”、“非极性”、“极性或非极性”)
(2)NH3与H2O分别能与H+ 结合成NH4+与H3O+。与NH4+具有相同空间构型的微粒是 ;
a、H3O+ b、CH4 c、P4 d、NH3
分子中的键角:CH4 P4(填:“>”、“=”或“< ”)。
(3)H3O+ 与NH4+ 的水溶液均显酸性。用离子方程式表示NH4+ 水溶液显酸性的原因:
。
(4)使用N、O、 B同位素,并结合水化学分析,将更有利于对测定结果的解释。写出B原子的最外层电子排布式 ;B原子核外的电子处在 个不同的能级上。
(1)关于14N与15N的正确说法是 ;
a、自然界氮元素中14N的含量:空气中大于地壳中 b、单质:14N2与15N2互为同位素
c、电子层结构:14N与15N完全相同 d、原子半径:14N小于15N
与N元素同周期且最外层有2个未成对电子的元素相互组成的化合物属于 分子。(填:“极性”、“非极性”、“极性或非极性”)
(2)NH3与H2O分别能与H+ 结合成NH4+与H3O+。与NH4+具有相同空间构型的微粒是 ;
a、H3O+ b、CH4 c、P4 d、NH3
分子中的键角:CH4 P4(填:“>”、“=”或“< ”)。
(3)H3O+ 与NH4+ 的水溶液均显酸性。用离子方程式表示NH4+ 水溶液显酸性的原因:
。
(4)使用N、O、 B同位素,并结合水化学分析,将更有利于对测定结果的解释。写出B原子的最外层电子排布式 ;B原子核外的电子处在 个不同的能级上。
 (2013?河东区一模)短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:
(2013?河东区一模)短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:(1)Y在元素周期表中的位置是
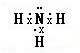
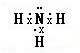
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈
(3)Y-AgO电池是应用广泛的鱼类电池,其原理如图所示.该电池的负极反应式是
(4)Z和W比较.非金属性较弱的是
a、元素在地壳中的含量
b、最高价氧化物对应水化物的酸性
c、断开氢化物中1molH-Z或H-W键所需的能量
d、Z与W以共价键形成化合物时,Z或W显示的电性
(5)含W的物质通常有漂白、杀菌作用.其中可作水消毒剂的有
(6)由Z和W组成的化合物遇水立即水解产生两种酸,写出此反应的化学方程式
(1)W元素在周期表中的位置为
(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于
(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44kJ热量,则该反应的热化学方程式为
 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下D与NaOH溶液反应的离子方程式
| ||
| ||
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
(5 )X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为