题目内容
2007年8月《地球学报》杂志报道,利用氮、氧及氮、硼同位素技术,通过测定可知地下硝酸盐来源的水污染情况。完成下列填空:
(1)关于14N与15N的正确说法是 ;
a、自然界氮元素中14N的含量:空气中大于地壳中 b、单质:14N2与15N2互为同位素
c、电子层结构:14N与15N完全相同 d、原子半径:14N小于15N
与N元素同周期且最外层有2个未成对电子的元素相互组成的化合物属于 分子。(填:“极性”、“非极性”、“极性或非极性”)
(2)NH3与H2O分别能与H+ 结合成NH4+与H3O+。与NH4+具有相同空间构型的微粒是 ;
a、H3O+ b、CH4 c、P4 d、NH3
分子中的键角:CH4 P4(填:“>”、“=”或“< ”)。
(3)H3O+ 与NH4+ 的水溶液均显酸性。用离子方程式表示NH4+ 水溶液显酸性的原因:
。
(4)使用N、O、 B同位素,并结合水化学分析,将更有利于对测定结果的解释。写出B原子的最外层电子排布式 ;B原子核外的电子处在 个不同的能级上。
(1)c(1分);极性或非极性(1分)(2)b、c(1分×2);﹥(1分)(3)NH4++H2O NH3·H2O+H+(1分)(4)2s22p1 (1分);3(1分)
NH3·H2O+H+(1分)(4)2s22p1 (1分);3(1分)
解析试题分析:(1)a、同位素原子在元素中所占的比例是不变的,所以自然界氮元素中14N的含量:空气中=地壳中,故a错误;b、14N2与15N2都是原子,不是同位素,故b错误;c、14N与15N的核外电子数都为7,电子层结构完全相同,故c正确;d、14N小于15N的核外电子数都为7,核外电子数相等,半径相等,故d错误;故选:c;先与N元素同周期且最外层有2个未成对电子的元素有C、O两种,形成的化合物有:CO和CO2;CO原子间以共价键结合,分子里电荷分布不均匀,正负电荷中心不重合,为极性分子;CO2原子间以共价键结合,分子里电荷分布均匀,正负电荷中心重合,为非极性分子,
故答案为:极性或非极性;(2)NH4+的空间结构为正四面体;H3O+、CH4、P4、NH3的空间结构为三角锥形、正四面体、正四面题、三角锥形,所以微粒与NH4+具有相同空间构型的微粒是CH4、P4,故选:b、c;CH4分子中键角为109.5°,P4分子中键角为69°,分子中的键角:CH4>P4,故答案为:>;(3)NH4+水解NH4++H2O?NH3?H2O+H+,使溶液呈酸性,故答案为:NH4++H2O?NH3?H2O+H+;(4)B原子的最外层电子数为3,最外层电子排布式为:2s22p1;B原子核外电子排布式:1S22s22p1,核外的电子处在3个不同的能级上,故答案为:2s22p1;3。
考点:本题主要考查了同位素、分子的极性、离子的空间结构,难度不大,注意知识的积累。

短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是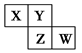
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
 Cl、
Cl、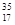 Cl为不同的核素,下列说法正确的是
Cl为不同的核素,下列说法正确的是
A. Cl2的摩尔质量是74 Cl2的摩尔质量是74 |
| B.通常情况下,氯气做氧化剂,但氯气也具有还原性 |
C. Cl、 Cl、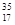 Cl互为同位素, Cl互为同位素,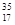 Cl2与 Cl2与 Cl2互为同素异形体 Cl2互为同素异形体 |
D.常温下,4.48L Cl2含有8NA个中子(NA为阿伏加德罗常数的值) Cl2含有8NA个中子(NA为阿伏加德罗常数的值) |
X.Y两种元素形成含氧酸A和B,能说明酸A比酸B强的是
| A.酸A中X的化合价比酸B中Y化合价高 |
| B.酸A中X与酸B中Y在同一周期,且X在Y之后 |
| C.酸A与酸B的铵盐溶液反应生成酸B |
| D.酸A具有强氧化性,酸B没有强氧化性 |
有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16。三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子。有关判断不正确的是
| A.X元素位于ⅥA族 |
| B.A不能溶解于B中 |
| C.B的沸点高于C的沸点 |
| D.A和C不可能发生氧化还原反应 |
下列叙述与对应图式正确的是
A.由下列短周期元素性质的数据推断③元素最高价氧化物对应的水化物碱性最强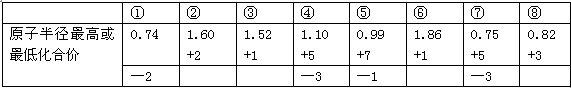 |
B.图甲表示Zn—Cu原电池反应过程中的电流强度的变化。T时可能加入了H2O2 |
| C.图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 |
| D.图丙表示元素周期表的一部分,元素X,Y,Z、W中X的氢化物酸性最强 |
下列说法不正确的是( )
| A.NH4+中质子数和电子数相等 |
| B.乙醇比乙二醇的沸点低 |
| C.乙炔与苯的实验式均为CH |
| D.过氧化钠与过氧化氢中均含有非极性键 |
X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,X+是一个裸露的质子,X和Z处于同一主族,Y、Z的最外层电子数之和与Q的最外层电子数相等,W的最内层电子数和最外层电子数之和等于次外层电子数。下列说法正确的是
| A.Y分别与X、Z以及W形成的化合物都不止一种 |
| B.原子半径:rQ>rW>rZ>rY>rX |
| C.化合物XQ和ZQ中化学键的类型相同 |
| D.Q的单质和水反应可生成两种酸 |