摘要:24.已知RO3的w(O)=60% .且R核内质子数等于中子数.则R元素在周期表中的位置是 .计算过程 .(相对原子质量:O.16, Na.23)
网址:http://m.1010jiajiao.com/timu3_id_212238[举报]
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1∶1和1∶2的两种离子化合物。
(1)W在元素周期表中的位置是____________ ,Z2Y的电子式是_____________。
(2)工业合成XQ3是放热反应。下列措施中既能加快反应速率,又能提高原料转化率的是_____________ 。
a.升高温度 b.加入催化剂 c.将XQ3及时分离出去 d.增大反应体系的压强
(3)2.24 L(标准状况)XQ3被200 mL 1 mol/L QXY3溶液吸收后,所得溶液中离子浓度从大到小的顺序是(离子符号用化学式表示)______________。
(4)有人设计将WQ4Y与Y2反应的化学能转化为电能,其工作原理如图所示,a极的电极反应式是_____________。
(1)W在元素周期表中的位置是____________ ,Z2Y的电子式是_____________。
(2)工业合成XQ3是放热反应。下列措施中既能加快反应速率,又能提高原料转化率的是_____________ 。
a.升高温度 b.加入催化剂 c.将XQ3及时分离出去 d.增大反应体系的压强
(3)2.24 L(标准状况)XQ3被200 mL 1 mol/L QXY3溶液吸收后,所得溶液中离子浓度从大到小的顺序是(离子符号用化学式表示)______________。
(4)有人设计将WQ4Y与Y2反应的化学能转化为电能,其工作原理如图所示,a极的电极反应式是_____________。

(5)已知一定量的W(s)单质能在Y2 (g)中燃烧,其可能的产物及能量关系如下图所示: 请写出一定条件下WY2(g) 与W(s)反应生成WY(g)的热化学方程式______________ 。

(6)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是____________。
查看习题详情和答案>>
以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):

请填写下列空白:
(1)已知0.5mol甲烷和0.5mol水蒸气在t℃,p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量.该反应的热化学方程式是:
(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气请应用化学反应速率和化学平衡的观点说明采取该措施的理由:
(3)当甲烷合成氨气的转化率为75%时,以5.60×107L甲烷为原料能够合成
(4)已知尿素的结构简式为 ,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
①
 ;②
;②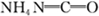
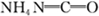 .
.
查看习题详情和答案>>

请填写下列空白:
(1)已知0.5mol甲烷和0.5mol水蒸气在t℃,p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量.该反应的热化学方程式是:
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2aKJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2aKJ/mol
.(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气请应用化学反应速率和化学平衡的观点说明采取该措施的理由:
增大氢气和氮气的浓度有利于增大反应速率,增大氢气和氮气浓度,减少氨气浓度有利于平衡正向进行
增大氢气和氮气的浓度有利于增大反应速率,增大氢气和氮气浓度,减少氨气浓度有利于平衡正向进行
(3)当甲烷合成氨气的转化率为75%时,以5.60×107L甲烷为原料能够合成
1.12×108
1.12×108
L氨气(假设体积均在标准状况下测定).(4)已知尿素的结构简式为
 ,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:①


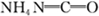
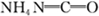
 (2013?辽宁一模)[化学--选修3物质结构与性质]
(2013?辽宁一模)[化学--选修3物质结构与性质]已知R、W、X、Y、Z是周期表中前四凰期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2+与W2-具有相同的电子层结构;Y元素原子的3p能级处于半充满状态;Z+的电子层都充满电子.请回答下列问题:
(1)写出Z的基态原子的外围电子排布式
3d104s1
3d104s1
.(2)R的某种钠盐晶体,其阴离子Am-(含R、W、氢三种元素)的球棍模型如图所示:在Am-中,R原子轨道杂化类型有
SP2、SP3
SP2、SP3
;m=2
2
.(填数字)(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子所构成的立体几何构型为
正八面体
正八面体
.(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]SO4,下列说法正确的是
AD
AD
A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(NH3)4]SO4中Z2+给出孤对电子,NH3提供空轨道
C.[Z(NH3)4]SO4组成元素中第一电离能最大的是氧元素
D.SO42-与PO43-互为等电子体,空间构型均为四面体
(5)固体YCl5的结构实际上是Ycl4+和YCl6-构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为apm,则晶胞的密度为
| 417×1030 |
| a3NA |
| 417×1030 |
| a3NA |
X、Y、Z、W为四种短周期主族元素,且原子序数依次增大.已知X的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最外层电子数是W原子最外层电子数的2倍,Z原子最外层只有一个电子.下列说法正确的是( )
查看习题详情和答案>>
已知X、Y、Z、W是元素周期表中前20号元素,其中Y和W处于相同周期,且能形成一种常被称为“臭碱”的化合物Y2W.X、Y、Z是金属元素,且原子序数依次增大,若由这3种元素构成的单质的物质的量记为n(X)、n(Y)、n(Z),它们与足量盐酸反应产生H2的体积(标准状况下)记为V(H2)X、V(H2)Y、V(H2)Z,且有下列关系:n(X)=n(Y)=(n)Z,2V(H2)X=V(H2)Y+V(H2)Z.试根据上述信息回答下列问题:
(1)Y2W的电子式为
 ,用离子方程式表示Y2W被称为“臭碱”的原因:
,用离子方程式表示Y2W被称为“臭碱”的原因:
(2)若Z为第3周期元素,则X在元素周期表中的位置是,单质X与单质Z的化学性质相似,试写出单质X与Y的最高价氧化物对应的水化物反应的化学方程式:
(3)若Z为第4周期元素,用化学方程式表示工业上制备单质Y的方法:
查看习题详情和答案>>
(1)Y2W的电子式为


S2-+H2O?HS-+OH-、HS-+H2O?H2S+OH-
S2-+H2O?HS-+OH-、HS-+H2O?H2S+OH-
.(2)若Z为第3周期元素,则X在元素周期表中的位置是,单质X与单质Z的化学性质相似,试写出单质X与Y的最高价氧化物对应的水化物反应的化学方程式:
Be+2NaOH=NaBeO2+H2↑
Be+2NaOH=NaBeO2+H2↑
.(3)若Z为第4周期元素,用化学方程式表示工业上制备单质Y的方法:
2NaCl(熔融)
2Na+Cl2↑
| ||
2NaCl(熔融)
2Na+Cl2↑
.已知Y的氢化物能与水剧烈反应生成一种气体单质,当有33.6L(标准状况下)气体生成时,反应中转移的电子数为
| ||
1.5NA
1.5NA
.