摘要:铜合金:各种铜合金的组成(青铜:_____,黄铜:_____.还含有少量锡.铅.铝等,白铜:含_____及少量锰).
网址:http://m.1010jiajiao.com/timu3_id_195270[举报]
(1)铜在一定条件下也能被腐蚀.下列图一装置中,铜腐蚀的速度最慢的是(填图一装置序号) ,装置I中观察到的现象是 .
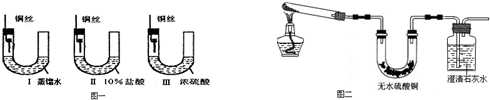
(2)金属铜长期暴露在潮湿空气中,往往被腐蚀成“铜绿”{碱式碳酸铜:[Cu2(OH)2CO3]},“铜绿”受热易分解.请预测“铜绿”分解的产物 .为验证“铜绿”分解的部分产物,某同学设计了图二装置:
图二装置可初步验证“铜绿”分解的产物,为验证分解的固体产物需要做补充实验,方法是 .
(3)为了从“铜绿”中制得铜,并测定“铜绿”的组成,把“铜绿”放在试管中,与通入的纯净氢气在加热条件下发生反应,实验装置如图三,请回答下列有关问题: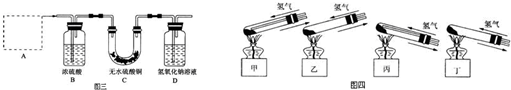
(i)A处应选用图四装置中的(填写编号) .
(ii)反应进行时,应先 再 .
(iii)要测定“铜绿”的组成,除需要知道样品质量外还需测定的实验数据是
(iv)上述装置还有不完善之处,请指出改正措施 、 .
查看习题详情和答案>>

(2)金属铜长期暴露在潮湿空气中,往往被腐蚀成“铜绿”{碱式碳酸铜:[Cu2(OH)2CO3]},“铜绿”受热易分解.请预测“铜绿”分解的产物
图二装置可初步验证“铜绿”分解的产物,为验证分解的固体产物需要做补充实验,方法是
(3)为了从“铜绿”中制得铜,并测定“铜绿”的组成,把“铜绿”放在试管中,与通入的纯净氢气在加热条件下发生反应,实验装置如图三,请回答下列有关问题:

(i)A处应选用图四装置中的(填写编号)
(ii)反应进行时,应先
(iii)要测定“铜绿”的组成,除需要知道样品质量外还需测定的实验数据是
(iv)上述装置还有不完善之处,请指出改正措施
[化学-选修/物质结构与性质]
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于 .
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为 .
(2)下表为元素周期表的一部分,根据此表回答下列问题:
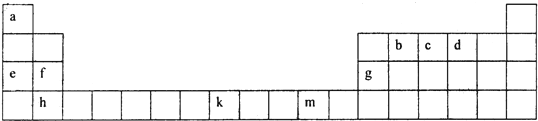
①f、g、h三种元素的第一电离能由小到大的顺序是 (用元素符号表示),b、c、d三种元素的电负性由大到小的顺序是 (用元素符号表示),b、c、d分别与a形成的简单化合物分子中,属于含有极性键的非极性分子是 .(填写化学式)
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式 .
目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为 .
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
,其中各原子的最外层电子均满足8电子稳定结构.该阴离子的中心原子的杂化轨道方式为 杂化,阴离子的电子式为 .
查看习题详情和答案>>
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为
(2)下表为元素周期表的一部分,根据此表回答下列问题:

①f、g、h三种元素的第一电离能由小到大的顺序是
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式

目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
3- 4 |
 [化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.
[化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.(1)写出Fe2+的核外电子排布式
(2)[cr(H2O)4Cl2]Cl?2H2O中cr的配位数为
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型
(4)常温下,碳与氢以原子个数比1:1形成的气态氢化物中,其分子中的σ键和П键的数目比是
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途.CuH的晶体结构如右图所示,若CuH的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞的边长为
为测定某铁铜合金的组成,现将5.6g该合金(表面氧化膜成分为Fe2O3和CuO)加入到过量稀硫酸中,完全反应后产生气体672mL,并得到浅绿色溶液A(不含Cu2+离子)和不溶物B.过滤,将B加入到适量的某浓度的硝酸中,完全溶解后,得NO、NO2的混合气896mL,经测定该混合气中V(NO):V(NO2)=3:1.再将A也加入到足量同浓度的硝酸中充分反应,用排水法收集产生的气体结果得一烧瓶气体,(不从水中移出烧瓶)紧接着向烧瓶中通入224mL O2,气体能恰好完全溶于水(以上所有气体体积都已换算成标准状况时的数据).下列结论正确的是( )
| A、合金中氧元素的物质的量是0.01 mol | B、合金中铁单质的质量是1.68 g | C、溶液A中存在的阳离子只有Fe2+离子 | D、不溶物B为铜单质且质量是1.6 g |