题目内容
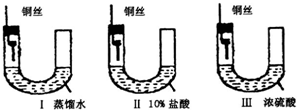
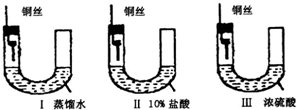
(1)铜在一定条件下也能被腐蚀.下列图一装置中,铜腐蚀的速度最慢的是(填图一装置序号)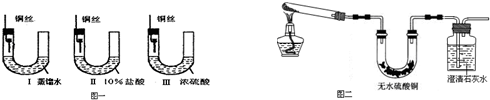
(2)金属铜长期暴露在潮湿空气中,往往被腐蚀成“铜绿”{碱式碳酸铜:[Cu2(OH)2CO3]},“铜绿”受热易分解.请预测“铜绿”分解的产物
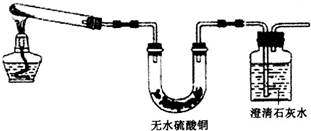
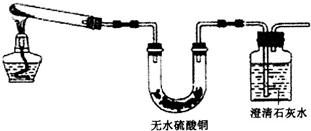
图二装置可初步验证“铜绿”分解的产物,为验证分解的固体产物需要做补充实验,方法是
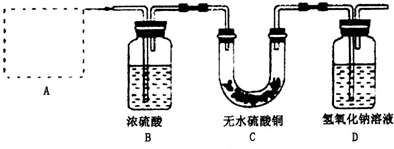
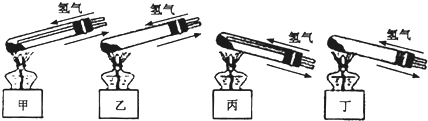
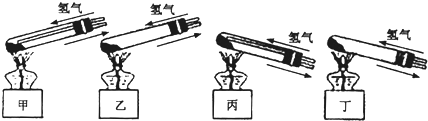
(3)为了从“铜绿”中制得铜,并测定“铜绿”的组成,把“铜绿”放在试管中,与通入的纯净氢气在加热条件下发生反应,实验装置如图三,请回答下列有关问题:
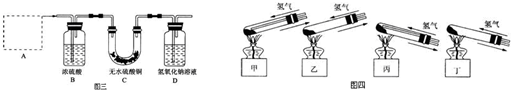
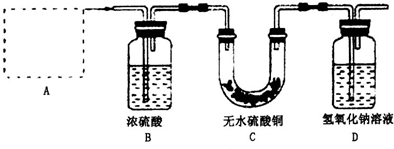
(i)A处应选用图四装置中的(填写编号)
(ii)反应进行时,应先
(iii)要测定“铜绿”的组成,除需要知道样品质量外还需测定的实验数据是
(iv)上述装置还有不完善之处,请指出改正措施
分析:(1)金属生锈的条件是:与氧气接触,有水参加,根据金属的吸氧腐蚀条件来回答;
(2)金属铜暴漏在潮湿的空气中,会和空气中的二氧化碳、水以及氧气发生化合反应生成碱式碳酸铜,碱式碳酸铜易分解,氧化铜是黑色易和酸反应的物质;
(3)(i)固体加热分解装置中的大试管要向下倾斜,并且氢气通入到药品的上方位置;
(ii)反应进行时,应先通气体再点灯,防止空气的干扰;
(iii)要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量;
(iv)实验要注意尾气处理装置的使用.
(2)金属铜暴漏在潮湿的空气中,会和空气中的二氧化碳、水以及氧气发生化合反应生成碱式碳酸铜,碱式碳酸铜易分解,氧化铜是黑色易和酸反应的物质;
(3)(i)固体加热分解装置中的大试管要向下倾斜,并且氢气通入到药品的上方位置;
(ii)反应进行时,应先通气体再点灯,防止空气的干扰;
(iii)要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量;
(iv)实验要注意尾气处理装置的使用.
解答:解:(1)金属生锈的条件是:与氧气接触,有水参加,图Ⅲ中浓硫酸具有吸水性,能减少水蒸气的量,可以减慢金属铜腐蚀的速率,装置I中金属铜发生吸氧腐蚀导致支管试管内气压增大排出导管内气体,致使图Ⅰ中管内因氧气减少而气压下降,所以该端液体上升;管内右端液体下降,故答案为:Ⅲ;U型管中左侧液面上升,右侧液面下降,铜丝表面变绿色;
(2)金属铜暴露在潮湿的空气中,会和空气中的二氧化碳、水以及氧气发生化合反应生成碱式碳酸铜,碱式碳酸铜易分解生成氧化铜、水以及二氧化碳,图二装置可初步验证“铜绿”分解的产物有水和二氧化碳,但是缺少氧化铜的检验,氧化铜可以和硫酸反应生成硫酸铜蓝色溶液,所以将反应后的黑色固体溶于足量的稀硫酸中,黑色固体完全溶解变成蓝色溶液,证明氧化铜的存在,故答案为:将反应后的黑色固体溶于足量的稀硫酸中,黑色固体完全溶解变成蓝色溶液;
(3)(i)给试管中的固体加热时,为了防止冷凝水倒流入试管底,使试管骤然遇冷而炸裂,大试管的管口应略向下倾斜,并且氢气通入到药品的上方位置,故答案为:D;
(ii)反应进行时,为了防止空气的干扰,应先通氢气再点燃酒精灯,故答案为:通入H2排净空气;点燃酒精灯加热;
(iii)要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量,故答案为:CO2、H2O和Cu的质量;
(iv)实验中要注意尾气的处理问题,对于剩余的氢气,可以将之点燃(或用气球收集),故答案为:将D装置中排出气体点燃;将D装置中排出气体用气球收集.
(2)金属铜暴露在潮湿的空气中,会和空气中的二氧化碳、水以及氧气发生化合反应生成碱式碳酸铜,碱式碳酸铜易分解生成氧化铜、水以及二氧化碳,图二装置可初步验证“铜绿”分解的产物有水和二氧化碳,但是缺少氧化铜的检验,氧化铜可以和硫酸反应生成硫酸铜蓝色溶液,所以将反应后的黑色固体溶于足量的稀硫酸中,黑色固体完全溶解变成蓝色溶液,证明氧化铜的存在,故答案为:将反应后的黑色固体溶于足量的稀硫酸中,黑色固体完全溶解变成蓝色溶液;
(3)(i)给试管中的固体加热时,为了防止冷凝水倒流入试管底,使试管骤然遇冷而炸裂,大试管的管口应略向下倾斜,并且氢气通入到药品的上方位置,故答案为:D;
(ii)反应进行时,为了防止空气的干扰,应先通氢气再点燃酒精灯,故答案为:通入H2排净空气;点燃酒精灯加热;
(iii)要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量,故答案为:CO2、H2O和Cu的质量;
(iv)实验中要注意尾气的处理问题,对于剩余的氢气,可以将之点燃(或用气球收集),故答案为:将D装置中排出气体点燃;将D装置中排出气体用气球收集.
点评:本题考查学生金属铜的腐蚀以及金属铜的化学性质,结合试验来考察增加了解题的难度.

练习册系列答案
相关题目
(1) 已知在一定条件下的反应4HCl+O2=2Cl2 +2H2O中, 有4mol HCl被氧化时,放出120kJ的热量,且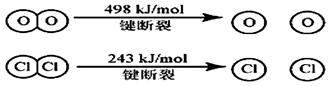
则断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差为__________KJ。
(2)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
(3)已知AlCl3熔点190℃,沸点183℃,结构如右图所示:AlCl3晶体内含有的作用力有 (填序号)。
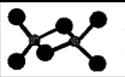
A.离子键 B.共价键 C.金属键
D.配位键 E.范德华力 F. 氢键
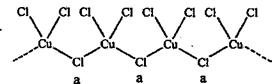
(4)氯和钾与不同价态的铜可生成两种化合物,这两种化合物中的阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 ,已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 。