摘要:18.已知Na2O2与CO2.H2O反应的方程式是: ①2Na2O2+2CO2=2Na2CO3+O2↑ ②2Na2O2+2H2O=4NaOH+O2↑ 将8.4 g的CO2和水蒸气混合气体.通入足量的Na2O2中.可得O2 4g.求原混合气体中CO2和水蒸气的质量.
网址:http://m.1010jiajiao.com/timu3_id_194393[举报]
已知Na2O2与CO2 、H2O反应的方程式是:
①2Na2O2+2CO2=2Na2CO3+O2 ;②2Na2O2+2H2O =4NaOH+O2↑
现将8.4 g CO2和H2O的混合气体,通入足量的Na2O2中,可得O2(标准状况)2.8 L,求原混合气体中CO2与H2O的物质的量各是多少?
查看习题详情和答案>>
已知Na2O2与CO2 、H2O反应的方程式是:①2Na2O2+2CO2=2Na2CO3+O2 ;
②2Na2O2+2H2O =4NaOH+O2↑ 将8.4 g 的CO2和H2O混合气体,通入足量的Na2O2中,可得O2(标准状况)2.8 L,求原混合气体中CO2的物质的量和H2O的质量?
查看习题详情和答案>>Na2O2是常见的氧化剂.某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.

[实验步骤]
I.按如图所示装置(部分仪器未画出)组装仪器,并检查装置气密性.
Ⅱ.将0.6g炭粉与3.9g Na2O2均匀混合,装入试管,在靠近试管口处放置一张湿润的氯化钯试纸(湿润氯化钯试纸遇CO变黑,可用于检验是否有CO生成).
Ⅲ、用酒精灯微微加热试管底部.
[实验现象]
试管中发生剧烈反应并产生火花,氯化钯试纸未变黑,石灰水未变浑浊.请回答:
(1)在图中方框内绘出仪器装置简图,使仪器装置图完整
 .
.
(2)装置B的作用是
(3)通过探究发现,装置A中发生的反应为2Na2O2+C
Na2CO3+X,X的电子式是
 .
.
(4)CO在潮湿环境中可将氯化钯还原为黑色粉末状的钯(Pd),同时生成另外两种物质.已知反应过程中转移6.02×l023个电子时,生成53g Pd,该反应的化学方程式为
(5)将装置A中充分反应后所得产物溶于适量水中.
①所得溶液的溶质是
②溶液中下列关系正确的是
a、c(Na+)>c(C
)>c(OH-)>c(HC
)
b、c(Na+)>c(OH-)>c(C
)>c(HC
)
c、c(Na+)=2c(C
)+c(HC
)+c(H2CO3)
d、c(H+)+c(Na+)=c(OH-)+2c(C
)+c(HC
)
③若使所得溶液与100mL稀盐酸恰好完全反应至溶液pH=7,该盐酸的物质的量浓度为
查看习题详情和答案>>

[实验步骤]
I.按如图所示装置(部分仪器未画出)组装仪器,并检查装置气密性.
Ⅱ.将0.6g炭粉与3.9g Na2O2均匀混合,装入试管,在靠近试管口处放置一张湿润的氯化钯试纸(湿润氯化钯试纸遇CO变黑,可用于检验是否有CO生成).
Ⅲ、用酒精灯微微加热试管底部.
[实验现象]
试管中发生剧烈反应并产生火花,氯化钯试纸未变黑,石灰水未变浑浊.请回答:
(1)在图中方框内绘出仪器装置简图,使仪器装置图完整


(2)装置B的作用是
防止倒吸
防止倒吸
.(3)通过探究发现,装置A中发生的反应为2Na2O2+C
| ||


(4)CO在潮湿环境中可将氯化钯还原为黑色粉末状的钯(Pd),同时生成另外两种物质.已知反应过程中转移6.02×l023个电子时,生成53g Pd,该反应的化学方程式为
PdCl2+CO+H2O=Pd+CO2+2HCl
PdCl2+CO+H2O=Pd+CO2+2HCl
.(5)将装置A中充分反应后所得产物溶于适量水中.
①所得溶液的溶质是
NaOH、Na2CO3
NaOH、Na2CO3
(填化学式).②溶液中下列关系正确的是
bd
bd
(填字母序号).a、c(Na+)>c(C
| O | 2- 3 |
| O | - 3 |
b、c(Na+)>c(OH-)>c(C
| O | 2- 3 |
| O | - 3 |
c、c(Na+)=2c(C
| O | 2- 3 |
| O | - 3 |
d、c(H+)+c(Na+)=c(OH-)+2c(C
| O | 2- 3 |
| O | - 3 |
③若使所得溶液与100mL稀盐酸恰好完全反应至溶液pH=7,该盐酸的物质的量浓度为
1mol/L
1mol/L
.图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
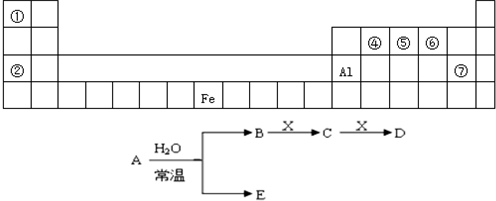
(1)若E为氧化物,则A与水反应的化学方程式为
①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为
(2)若E为单质气体,D为白色沉淀,A的化学式可能是
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该可逆反应的化学方程式为
查看习题详情和答案>>

(1)若E为氧化物,则A与水反应的化学方程式为
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
,该反应中氧化剂和还原剂的物质的量之比为1:2
1:2
.①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
.②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为
3Fe+8H++2NO3-═2Fe3++2NO↑+4H2O
3Fe+8H++2NO3-═2Fe3++2NO↑+4H2O
.(2)若E为单质气体,D为白色沉淀,A的化学式可能是
Na、Na2O2等
Na、Na2O2等
,B含有的化学键类型为离子键、共价键
离子键、共价键
,C与X反应的离子方程式为3AlO2-+Al3++6H2O═4Al(OH)3↓
3AlO2-+Al3++6H2O═4Al(OH)3↓
.(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该可逆反应的化学方程式为
CO+H2O
CO2+H2
| 高温 |
CO+H2O
CO2+H2
.| 高温 |
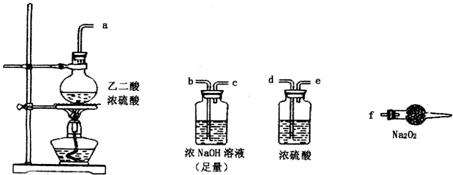
 有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:(1)第一小组同学设计如图装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,则反应的化学方程式为
2Na2O2+2SO2=2Na2SO3+O2
2Na2O2+2SO2=2Na2SO3+O2
.乙同学认为Na2O:与SO2反应除了生成Na2SO3和O2外,还有Na2SO.生成.为检验是否有Na2SO4生成,该同学设计了如下方案:
你认为乙同学的方案是否合理
否
否
(答“是”或“否”);请简要说明两点理由:①
稀HNO3可以把BaSO3氧化为BaSO4
稀HNO3可以把BaSO3氧化为BaSO4
②若反应后的固体有Na2O2残留,溶于水后可把SO32- 氧化为 SO42-
若反应后的固体有Na2O2残留,溶于水后可把SO32- 氧化为 SO42-
.(2)第二小组同学利用下图中的有关装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应.已知:H2C204
| ||
| △ |
Na2CO3
Na2CO3
;验证该产物可选择的试剂是稀H2SO4(或稀HC1)和澄清石灰水
稀H2SO4(或稀HC1)和澄清石灰水
.上述实验中选择的最简单的装置接口连接顺序为abcf
abcf
.