摘要:乙醇分子中不同的化学键如图.乙醇在一定条件下脱水能生成乙烯.下列关于乙醇 在各种不同反应里断裂键的说法错误的是 ( ) A.和金属Na反应.化学键①断裂 B.和金属Na反应.化学键②断裂 C.乙醇制乙烯的反应.化学键②⑤断裂 D.乙醇制乙醛的反应.化学键①③断裂
网址:http://m.1010jiajiao.com/timu3_id_173748[举报]
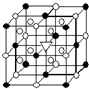 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子AlF6-
AlF6-
、Na+
Na+
;大立方体的体心处▽所代表的是AlF6-
AlF6-
.冰晶石在化工生产中的用途电解炼铝的助熔剂
电解炼铝的助熔剂
.(2)H2S和H2O2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
H2O2分子间存在氢键,与水分子可形成氢键
H2O2分子间存在氢键,与水分子可形成氢键
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.写出铜原子价电子层的电子排布式
3d104s1
3d104s1
,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有Cr
Cr
(填元素符号).实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有共价键和配位键
共价键和配位键
.实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4?H2O晶体.实验中所加C2H5OH的作用是降低Cu(NH3)4SO4?H2O的溶解度
降低Cu(NH3)4SO4?H2O的溶解度
.B.用含少量铁的氧化铜制取氯化铜晶体(CuCl2?xH2O).有如下操作:
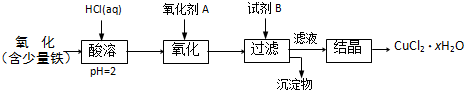
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解.
(1)加热酸溶过程中发生反应的离子方程式有:
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
(2)氧化剂A可选用
①
①
(填编号,下同)①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用
③
③
①NaOH ②FeO ③CuO
(4)试剂B的作用是
①③
①③
①提高溶液的pH ②降低溶液的pH ③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是
②④①
②④①
(按实验先后顺序填编号)①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g.
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g.
试评价上述两种实验方案,其中正确的方案是
二
二
,据此计算得x=| 80m-135n |
| 18n |
| 80m-135n |
| 18n |
 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.(1)工业上,可以分离合成气中的氢气,用于合成氨,常用醋酸二氨合亚铜[Cu(NH3)2]AC溶液(AC=CH3COO-)来吸收合成气中的一氧化碳,其反应原理为:[Cu(NH3)2]AC(aq)+CO(g)+NH3(g)?[Cu(NH3)3]AC?CO(aq)△H<0常压下,将吸收一氧化碳的溶液处理重新获得[Cu(NH3)2]AC溶液的措施是
(2)工业上一般采用下列两种反应合成甲醇:
反应a:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol;反应b:CO(g)+2H2(g)?CH3OH(g)△H<0
①对于反应a,某温度下,将4.0mol CO2(g)和12.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,测得甲醇蒸气的体积分数为30%,则该温度下反应的平衡常数为
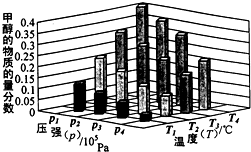
②对于反应b,某温度下,将1.0mol CO(g)和2.0mol H2(g)充入固定容积的密闭容器中,反应到达平衡时,改变温度和压强,平衡体系中CH3OH的物质的量分数变化情况如图所示,于温和压强的关系判断正确的是
A.p3>p2,T3>T2 B.p2>p4,T4>T2 C.p1>p3,T1>T3 D.p1>p4,T2>T3
(3)CO可以合成二甲醚,二甲醚可以作为燃料电池的原料,化学反应原理为:CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H<0
①在恒容密闭容器里按体积比为1:4充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是
A.逆反应速率先增大后减小
B.反应物的体积百分含量减小
C.正反应速率先增大后减小
D.化学平衡常数K值增大
②写出二甲醚碱性燃料电池的负极电极反应式
③己知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量.关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是
A.两种燃料互为同分异构体,分子式和摩尔质量相同,比能量相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
(4)已知lg二甲醚气体完全燃烧生成稳定的氧化物放出的热量为31.63kJ,请写出表示二甲醚燃烧热的热化学方程式
紫杉醇(paclitaxel)是一种抗癌药,化合物D是紫杉醇的侧链,D的合成路线如图甲:
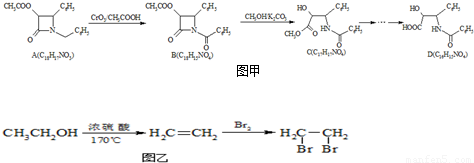
(1)A的合成应用了2010年诺贝尔化学奖的获奖成果--交叉偶联反应,反应式如下(已配平):
CH3COOCH2COCl+X A+HCl,X分子中含碳氮双键(C=N),其结构简式为______.
A+HCl,X分子中含碳氮双键(C=N),其结构简式为______.
(2)已知酯和酰胺在过量醇中能发生醇解反应:
CH3COOC2H5+CH3OH CH3COOCH3+C2H5OH
CH3COOCH3+C2H5OH
CH3CO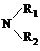 +CH3OH
+CH3OH CH3COOCH3+H
CH3COOCH3+H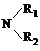
“醇解反应”的反应类型为______,B转化为C中另一产物的结构简式为______.
(3)若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F.
①E在一定条件下能发生缩聚反应,写出所得高分子化合物的一种可能的结构简式:______;
②F的同分异构体中,属于芳香族化合物、能发生银镜反应且核磁共振氢谱有4个峰的有两种,请写出其中一种的结构简式:______.
(4)已知:①RCHO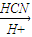
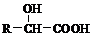
②R′COOH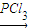 R′COCl
R′COCl
写出以甲醛和乙醛为原料合成CH3COOCH2COCl的路线流程图(无机试剂任选).合成路线流程图示例如图乙.
查看习题详情和答案>>

(1)A的合成应用了2010年诺贝尔化学奖的获奖成果--交叉偶联反应,反应式如下(已配平):
CH3COOCH2COCl+X
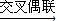 A+HCl,X分子中含碳氮双键(C=N),其结构简式为______.
A+HCl,X分子中含碳氮双键(C=N),其结构简式为______.(2)已知酯和酰胺在过量醇中能发生醇解反应:
CH3COOC2H5+CH3OH
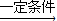 CH3COOCH3+C2H5OH
CH3COOCH3+C2H5OHCH3CO
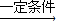 CH3COOCH3+H
CH3COOCH3+H“醇解反应”的反应类型为______,B转化为C中另一产物的结构简式为______.
(3)若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F.
①E在一定条件下能发生缩聚反应,写出所得高分子化合物的一种可能的结构简式:______;
②F的同分异构体中,属于芳香族化合物、能发生银镜反应且核磁共振氢谱有4个峰的有两种,请写出其中一种的结构简式:______.
(4)已知:①RCHO
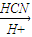
②R′COOH
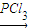 R′COCl
R′COCl写出以甲醛和乙醛为原料合成CH3COOCH2COCl的路线流程图(无机试剂任选).合成路线流程图示例如图乙.
查看习题详情和答案>>
(2011?崇川区三模)紫杉醇(paclitaxel)是一种抗癌药,化合物D是紫杉醇的侧链,D的合成路线如图甲:

(1)A的合成应用了2010年诺贝尔化学奖的获奖成果--交叉偶联反应,反应式如下(已配平):
CH3COOCH2COCl+X
A+HCl,X分子中含碳氮双键(C=N),其结构简式为
 .
.
(2)已知酯和酰胺在过量醇中能发生醇解反应:
CH3COOC2H5+CH3OH
CH3COOCH3+C2H5OH
CH3CO +CH3OH
+CH3OH
CH3COOCH3+H
“醇解反应”的反应类型为
(3)若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F.
①E在一定条件下能发生缩聚反应,写出所得高分子化合物的一种可能的结构简式: 或
或
 或
或 ;
;
②F的同分异构体中,属于芳香族化合物、能发生银镜反应且核磁共振氢谱有4个峰的有两种,请写出其中一种的结构简式: 或
或
 或
或 .
.
(4)已知:①RCHO

②R′COOH
R′COCl
写出以甲醛和乙醛为原料合成CH3COOCH2COCl的路线流程图(无机试剂任选).合成路线流程图示例如图乙.
查看习题详情和答案>>

(1)A的合成应用了2010年诺贝尔化学奖的获奖成果--交叉偶联反应,反应式如下(已配平):
CH3COOCH2COCl+X
| 交叉偶联 |


(2)已知酯和酰胺在过量醇中能发生醇解反应:
CH3COOC2H5+CH3OH
| 一定条件 |
CH3CO
 +CH3OH
+CH3OH| 一定条件 |

“醇解反应”的反应类型为
取代反应
取代反应
,B转化为C中另一产物的结构简式为CH3COOCH3
CH3COOCH3
.(3)若最后一步水解的条件控制不好,D会继续水解生成氨基酸E和芳香酸F.
①E在一定条件下能发生缩聚反应,写出所得高分子化合物的一种可能的结构简式:
 或
或
 或
或
②F的同分异构体中,属于芳香族化合物、能发生银镜反应且核磁共振氢谱有4个峰的有两种,请写出其中一种的结构简式:
 或
或
 或
或
(4)已知:①RCHO
| HCN |
| H+ |

②R′COOH
| PCl3 |
写出以甲醛和乙醛为原料合成CH3COOCH2COCl的路线流程图(无机试剂任选).合成路线流程图示例如图乙.
填空题
(1)列叙述正确的是______(填写序号)
A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗.
B.乙醛和新制氢氧化铜的反应实验要有明显现象,必须在强碱性条件下加热煮沸.
C.只有碳、氢两种元素组成的有机化合物称为烃.
D.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体.
E.乙烯、乙醇和乙醛均能发生加成反应.
F.浓溴水滴入苯酚溶液中能产生2,4,6-三溴苯酚的白色沉淀.
G.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,该现象能说明苯和溴的取代反应是放热反应.
(2)乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是:(填写序号)
①和金属钠作用时,断裂______;
②和浓硫酸共热至170℃时,断裂______;
③在铜催化下和氧气反应时,断裂______;
④与氢卤酸反应时,断裂______.
查看习题详情和答案>>
(1)列叙述正确的是______(填写序号)
A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗.
B.乙醛和新制氢氧化铜的反应实验要有明显现象,必须在强碱性条件下加热煮沸.
C.只有碳、氢两种元素组成的有机化合物称为烃.
D.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体.
E.乙烯、乙醇和乙醛均能发生加成反应.
F.浓溴水滴入苯酚溶液中能产生2,4,6-三溴苯酚的白色沉淀.
G.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,该现象能说明苯和溴的取代反应是放热反应.
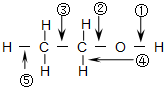
(2)乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是:(填写序号)
①和金属钠作用时,断裂______;
②和浓硫酸共热至170℃时,断裂______;
③在铜催化下和氧气反应时,断裂______;
④与氢卤酸反应时,断裂______.
