网址:http://m.1010jiajiao.com/timu3_id_173366[举报]

请回答下列问题:
(1)F的结构简式为


(2)物质A的名称是
(3)测定D中所含官能团的物理方法是
(4)B→C的化学方程式为


①2H2(g)+CO(g)?CH3OH(g);△H=-91.8kJ?mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ?mol
②CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ?mol
回答下列问题:
(2)水煤气合成二甲醚三步反应总的热化学方程式为:
(3)-定条件下的密闭容器中,该总反应达到平衡后,要提高CO的转化率,下列措施中可以采取的是
a.升高温度; b.降低温度; c.增大压强; d.减小压强;
e.缩小体积;f.增大CO的浓度;g.增大CO2的浓度
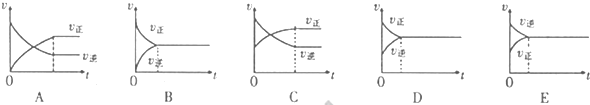
(3)某温度下,将一定里的CH3OH加入密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g),
经20min反应达到平衡,此时测得c(CH3OH)=0.56mol?L;c(H2O)=0.72mol?L-1
①达平衡时,c(CH3OCH3)=
②在相同的条件下,若起始浓度的数值如下表所示
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.28 | 0.86 | 0.86 |
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3;2SO2(g)+O2(g)![]() 2SO3(g)某温度下,SO2的平衡化率(α)与体系总压强(p)的关系如下图所示。根据图示回答下列问题。
2SO3(g)某温度下,SO2的平衡化率(α)与体系总压强(p)的关系如下图所示。根据图示回答下列问题。
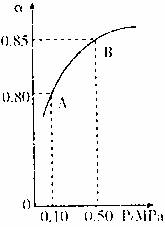
①平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”、“=”)。
②已知上述反应的是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列选项中有利于提高SO2平衡转化率的有 (填字母)。
A.升高温度 B.降低温度 C.增大压强
D.减小压强 E.加入催化剂 F.移出氧气
③SO2尾气用Na2SO3溶液吸收可得到重要化工原料,反应的化学方程式为
;上述反应产物的水溶液呈酸性,原因 。
④工业制硫酸中SO2的一种制法是煅烧FeS2制取,煅烧FeS2的产物之一Fe3O4溶于H2SO4后,加入Fe粉可制取FeSO4,酸溶过程需保持溶液足够酸性,其原因是
。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
若用标准状况下4.48L CH4还原NO2至N2的整个过程中转移的电子总数为
(阿伏加德罗常的值用NA表示),写出上述反应的热化学方程式:
。
查看习题详情和答案>>(1)F元素在周期表中的位置为
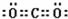
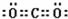
(2)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为
(3)科学研究证明:化学反应热只与始终态有关,与过程无关.单质B的燃烧热为a kJ/mol.由B、C二种元素组成的化合物BC 14g完全燃烧放出热量b kJ,写出单质B和单质C反应生成BC的热化学方程式
| 1 |
| 2 |
| 1 |
| 2 |
(4)1mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为

(1)元素K的原子中未成对电子数是
(2)这些元素中第一电离能最大的是
(3)A、B、C三种元素形成的一种化合物叫三聚氰胺(结构如图2),由于其含氮量相当高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石.三聚氰胺中二种环境的N原子的杂化形式分别是
(4)有下列物质①CA3;②GA3;③EH;④JH;⑤FD2.请将这些物质的熔点由高到低排列