摘要:下列反应硫酸表现氧化性的是: A.室用浓硫酸干燥氯气.氯化氢等气体 B.KI与浓硫酸混合.有紫色蒸气产生 C.硫酸与氧化亚铁反应.会生成硫酸铁 D.浓硫酸在木制品上“烙 字画
网址:http://m.1010jiajiao.com/timu3_id_163605[举报]
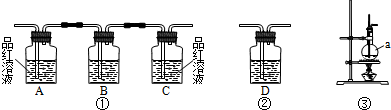
实验室用浓硫酸和乙醇混合加热制取乙烯,常因温度过高而发生副反应生成一定量的二氧化硫.请用下图装置设计一个实验,验证上述反应所得混合气体中含有乙烯和二氧化硫,并回答:
(1)实验仪器a的名称是 .
(2)制备乙烯的化学方程式为:CH3CH2OH
.
(3)装置的连接顺序为(用编号按气流从左到右表示) ,D瓶中应盛放下列试剂中的 (填字母代号)
A.NaOH溶液 B.浓硫酸 C.酸性KMnO4溶液 D.溴水
(4)能说明SO2气体存在的现象是 ,使用装置B的目的是 .
(5)能验证原混合气体中含有乙烯的现象是 ,并简述理由: .
 查看习题详情和答案>>
查看习题详情和答案>>
(1)实验仪器a的名称是
(2)制备乙烯的化学方程式为:CH3CH2OH
| 浓硫酸 | 170℃ |
(3)装置的连接顺序为(用编号按气流从左到右表示)
A.NaOH溶液 B.浓硫酸 C.酸性KMnO4溶液 D.溴水
(4)能说明SO2气体存在的现象是
(5)能验证原混合气体中含有乙烯的现象是
 查看习题详情和答案>>
查看习题详情和答案>>
下列说法正确的是( )
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
C.Cl-存在时,铝表面的氧化膜易被破坏,因此含盐腌制食品不宜直接存放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
查看习题详情和答案>>
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
C.Cl-存在时,铝表面的氧化膜易被破坏,因此含盐腌制食品不宜直接存放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
查看习题详情和答案>>
浓硫酸表现的性质为:
A、高沸点
B、强酸性
C、吸水性
D、脱水性
E、强氧化性.在下列用途或反应中:
(1)热的浓硫酸与木炭反应;
(2)实验室制氯化氢气体;
(3)干燥氢气;
(4)热的浓硫酸溶解铜;
(5)浓硫酸可用钢瓶储运;
(6)泄漏到地面的浓硫酸洒上生石灰处理;
(7)浓硫酸使蔗糖变黑.用编号填空:
①仅体现出吸水性的是________;
②仅表现出强酸性的是________;
③既表现出强酸性又表现出强氧化性的是________,其反应方程式为________.
高纯氧化铁(α-Fe2O3)是现代电子工业的重要材料.实验室用硫铁矿烧渣(主要成分为Fe2O3、FeO,还含有SiO2等杂质)为原料制备高纯氧化铁的步骤如下:
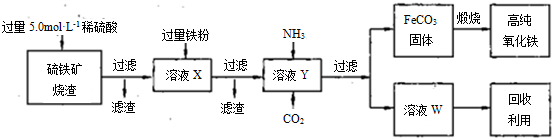
回答下列问题:
(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应.写出该反应的离子方程式: .
(2)实验室欲用18.4mol?L-1的浓硫酸配制100mL 5.0mol?L-1的硫酸溶液,所用的玻璃仪器胶头滴管、量筒、烧杯、玻璃棒外,还有 (填写仪器名称).
(3)某同学用如图1所示装置进行过滤操作.
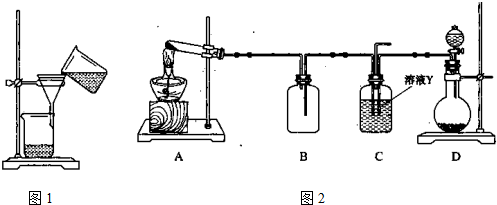
①请指出其中的错误之处: ;
②过滤后,洗涤过滤器中少量沉淀的方法是 .
(4)某同学用图2所示实验装置(尾气吸收装置未画出)向溶液Y中通入NH3和CO2.
①下列为实验室制备NH3和CO2的备选药品:
a.NH4Cl b.CaCO3(块状) c.Ca(OH)2 d.NaOH e.浓氨水 f.稀盐酸 g.稀硫酸
则上述装置A处的试管中所放药品的最佳选择为 和 (用药品序号填空);装置D处药品的最佳选择为 和 (用药品序号填空).
②下列各项制备实验中,也可利用装置D处仪器完成的是 (填序号).
A.MnO2与浓盐酸反应制备Cl2
B.Cu与浓硫酸反应生成SO2
C.由KMnO4分解制O2
D.乙醇与乙酸反应制备乙酸乙酯
E.Zn与稀硫酸反应制备H2
③写出上述装置A处的试管中所发生反应的化学方程式 .
④若通入一定量的NH3和CO2后,装置C处的溶液中只含有S、N、H、O四种元素.用pH试纸测定该溶液pH的方法是 ;若该溶液呈中性,则溶液中的NH4+和SO42-的物质的量浓度间的数量关系为 .(离子的浓度用符号[NH4+]和[SO42-]表示)
查看习题详情和答案>>

回答下列问题:
(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应.写出该反应的离子方程式:
(2)实验室欲用18.4mol?L-1的浓硫酸配制100mL 5.0mol?L-1的硫酸溶液,所用的玻璃仪器胶头滴管、量筒、烧杯、玻璃棒外,还有
(3)某同学用如图1所示装置进行过滤操作.

①请指出其中的错误之处:
②过滤后,洗涤过滤器中少量沉淀的方法是
(4)某同学用图2所示实验装置(尾气吸收装置未画出)向溶液Y中通入NH3和CO2.
①下列为实验室制备NH3和CO2的备选药品:
a.NH4Cl b.CaCO3(块状) c.Ca(OH)2 d.NaOH e.浓氨水 f.稀盐酸 g.稀硫酸
则上述装置A处的试管中所放药品的最佳选择为
②下列各项制备实验中,也可利用装置D处仪器完成的是
A.MnO2与浓盐酸反应制备Cl2
B.Cu与浓硫酸反应生成SO2
C.由KMnO4分解制O2
D.乙醇与乙酸反应制备乙酸乙酯
E.Zn与稀硫酸反应制备H2
③写出上述装置A处的试管中所发生反应的化学方程式
④若通入一定量的NH3和CO2后,装置C处的溶液中只含有S、N、H、O四种元素.用pH试纸测定该溶液pH的方法是
实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷(BrCH2CH2Br).
反应分两步进行:
第一步,乙醇与浓硫酸共热到170℃生成乙烯(CH3CH2OH
CH2=CH2↑+H2O);
第二步,乙烯与溴生成1,2-二溴乙烷(CH2=CH2+Br2→BrCH2CH2Br).
可能存在的副反应有:乙醇在浓硫酸的存在下于l40℃脱水生成乙醚(C2H5-O-C2H5);温度过高,乙醇与浓硫酸反应生成SO2、CO2等酸性气体.
有关数据列表如下:
反应装置如图(略去加热等装置):
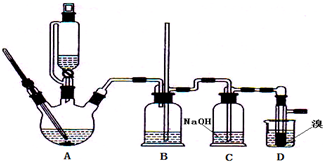
回答下列问题:
(1)熔沸点:乙醇>乙醚.利用物质结构的相关知识解释原因 .
(2)组装好仪器后检查A、B、C装置气密性的操作是 .
(3)如果D中导气管发生堵塞事故,装置B中可能观察到的现象是 .
(4)装置C中可能发生反应的化学方程式是 (写出一个即可).
(5)将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在 层(填“上”、“下”);若产物中有少量未反应的Br2,最好用 洗涤除去(填字母).
a.水 b.氢氧化钠溶液 c.乙醇
(6)若产物中有少量副产物乙醚,可采用的除杂方法是 .
(7)反应时装置D的烧杯中应装 (填“a”或“b”),不装另一种的原因是 .
a.冷水 b.冰水. 查看习题详情和答案>>
反应分两步进行:
第一步,乙醇与浓硫酸共热到170℃生成乙烯(CH3CH2OH
| H2SO4(浓) |
| 170℃ |
第二步,乙烯与溴生成1,2-二溴乙烷(CH2=CH2+Br2→BrCH2CH2Br).
可能存在的副反应有:乙醇在浓硫酸的存在下于l40℃脱水生成乙醚(C2H5-O-C2H5);温度过高,乙醇与浓硫酸反应生成SO2、CO2等酸性气体.
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 色、态 | 无色液体 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/(g?cm-3) | 0.79 | 2.2 | 0.71 | 3.1 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 59.47 |
| 熔点/℃ | -130 | 9 | -116 | -7.25 |

回答下列问题:
(1)熔沸点:乙醇>乙醚.利用物质结构的相关知识解释原因
(2)组装好仪器后检查A、B、C装置气密性的操作是
(3)如果D中导气管发生堵塞事故,装置B中可能观察到的现象是
(4)装置C中可能发生反应的化学方程式是
(5)将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
a.水 b.氢氧化钠溶液 c.乙醇
(6)若产物中有少量副产物乙醚,可采用的除杂方法是
(7)反应时装置D的烧杯中应装
a.冷水 b.冰水. 查看习题详情和答案>>