摘要:37.现有一瓶标签如图所示的浓盐酸.请根据标签上的数据回答问题: (1)要配制165g.20%的盐酸.需用该浓盐酸 mL. (2)利用刚配制的稀盐酸来测定某碳酸盐样品的纯度:取一定量该碳酸盐(R2C03)样品.向其中滴入刚配好的稀盐酸至不再产生气泡为止.共用去盐酸73g(杂质不与盐酸 反应也不溶于水).然后过滤.得滤渣2.8g.将所得滤液蒸干.得到固体纯净物23.4g. ①发生反应的化学方程式. ②该样品的主要成分化学式的是 ③利用已知条件求解参加反应的固体物质质量(x)的比例式 ④该样品的纯度是 ⑤若向反应后溶液中加入31,6g水后.此时所得溶液中溶质的质量分数为 2010年山东省泰安市新泰第一教研区中考预测卷(四)
网址:http://m.1010jiajiao.com/timu3_id_16017[举报]
现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题:
(1)要配制165g.20%的盐酸,需用该浓盐酸 mL.
(2)利用刚配制的稀盐酸来测定某碳酸盐样品的纯度(不含氢元素):取一定量该碳酸盐(R2C03)样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸73g(杂质不与盐酸反应也不溶于水),然后过滤,得滤渣2.8g,将所得滤液蒸干,得到固体纯净物23.4g.
①发生反应的化学方程式. ②该样品的主要成分化学式的是
③利用已知条件求解参加反应的固体物质质量(x)的比例式
④该样品的纯度是
⑤若向反应后溶液中加入31.6g水后,此时所得溶液中溶质的质量分数为 .
查看习题详情和答案>>
| 盐酸 体积:500mL 化学式:HCl 相对分子质量:36.5 密度:1.1g/cm3 质量分数:30% |
(2)利用刚配制的稀盐酸来测定某碳酸盐样品的纯度(不含氢元素):取一定量该碳酸盐(R2C03)样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸73g(杂质不与盐酸反应也不溶于水),然后过滤,得滤渣2.8g,将所得滤液蒸干,得到固体纯净物23.4g.
①发生反应的化学方程式.
③利用已知条件求解参加反应的固体物质质量(x)的比例式
④该样品的纯度是
⑤若向反应后溶液中加入31.6g水后,此时所得溶液中溶质的质量分数为
 现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题:
现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题:(1)要配制165g.20%的盐酸,需用该浓盐酸
(2)利用刚配制的稀盐酸来测定某碳酸盐样品的纯度(不含氢元素):取一定量该碳酸盐(R2C03)样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸73g(杂质不与盐酸 反应也不溶于水),然后过滤,得滤渣2.8g,将所得滤液蒸干,得到固体纯净物23.4g.
①发生反应的化学方程式
②该样品的主要成分化学式的是
③利用已知条件求解参加反应的固体物质质量(x)的比例式
④该样品的纯度是
⑤若向反应后溶液中加入31.6g水后,此时所得溶液中溶质的质量分数为
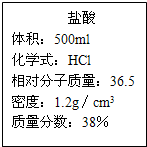 现有一瓶标签如图所示的浓盐酸,请根据标签完成下列问题:
现有一瓶标签如图所示的浓盐酸,请根据标签完成下列问题:(1)用该盐酸50mL能配制质量分数为20%的盐酸
(2)利用刚配制好的盐酸来测定某纯碱样品的纯度:取25g该纯碱样品,向其中滴入刚配制好的盐酸至不再产生气泡为止(样品中杂质不与盐酸反应),共用去盐酸73g,然后将溶液蒸干,得到固体27.2g.求该样品的纯度. 查看习题详情和答案>>
现有一瓶标签如图所示的浓盐酸,请根据标签上的数据回答问题:
| 盐酸 体积:500mL 化学式:HCl 相对分子质量:36.5 密度:1.2g/cm3 质量分数:37%(1)用该浓盐酸100ml能配制质量分数为20%的盐酸 (2)利用刚配制的稀盐酸来测定某碳酸钠样品的纯度(样品不含氢元素):取50g该样品,向其中滴入刚配好的稀盐酸至不再产生气泡为止,共用去盐酸146g. ①发生反应的化学方程式 ②利用已知条件求解参加反应的固体物质质量(x)的比例式 ③该样品的成分是 ④该样品的纯度是 ⑤若向反应后溶液中加入46.8g水后,此时所得溶液中溶质的质量分数为 |
 现有一瓶标签如图所示的浓盐酸,请根据标签完成下列问题:
现有一瓶标签如图所示的浓盐酸,请根据标签完成下列问题: