摘要:是一种新型无机材料.广泛应用与集成电路生产领域.某氮化铝中含有碳或氧化铝杂质.现用图Ⅰ中的一些装置来进行检验.使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O=NaAlO2+NH3↑.根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数.并根据实验现象来确定杂质的成分(实验中导管体积忽略不计) ⑴实验有关操作为:a.往锥形瓶中放入适量的AlN样品:b.从分液漏斗往锥形瓶中加入过量的浓NaOH,c.检验装置的气密性,d.测定收集到水的体积.正确的操作顺序为 . ⑵本试验中检查装置气密性的方法是 . ⑶广口瓶中的试剂X可选用 .A 汽油 B 酒精 C 植物油 D CCl4 ⑷广口瓶的液体没有装满.实验测得NH3的体积将 . ⑸实验结束后.若观察到锥形瓶中还有固体.则样品中含有的杂质是 . ⑹若实验中测得样品的质量为wg.氨气的体积为aL.则样品中AlN的质量分数为 (AlN的相对分子质量为41.每22.4L氨气质量为17g). ⑺有人改用图Ⅱ装置进行同样实验.通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行? (填入“可行 .“不可行 ).原因是 .改进的方法为 . ⑻在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液.然后边搅拌边逐滴向其中加入硫酸镁溶液.至溶液的红色完全褪去时.滤去沉淀.称得剩余溶液总质量为3mg . ①计算所加硫酸镁溶液的质量分数, ②用N表示溶液中离子的数目.不同种离子用离子符号注明[如N (Na')表示钠离子的数目].请建立坐标系.绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图.
网址:http://m.1010jiajiao.com/timu3_id_15328[举报]
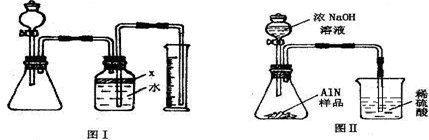
氮化铝(AlN)是一种新型无机材料,广泛应用与集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,现用图Ⅰ中的一些装置来进行检验,使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O=NaAlO2+NH3↑,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
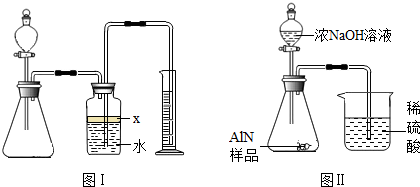
(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为 .
(2)本试验中检查装置气密性的方法是 .
(3)广口瓶中的试剂X可选用 (填选项的标号).A 汽油 B 酒精 C 植物油 D CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将 (填偏大、偏小或不变).
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是 .
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为 (AlN的相对分子质量为41,每22.4L氨气质量为17g).
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行? (填入“可行”、“不可行”).原因是 ,改进的方法为 .
(8)在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液,然后边搅拌边逐滴向其中加入硫酸镁溶液,至溶液的红色完全褪去时,滤去沉淀,称得剩余溶液总质量为3mg.
①计算所加硫酸镁溶液的质量分数;
②用N表示溶液中离子的数目,不同种离子用离子符号注明[如N (Na')表示钠离子的数目],请建立坐标系,绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图. 查看习题详情和答案>>

(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为
(2)本试验中检查装置气密性的方法是
(3)广口瓶中的试剂X可选用
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
(8)在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液,然后边搅拌边逐滴向其中加入硫酸镁溶液,至溶液的红色完全褪去时,滤去沉淀,称得剩余溶液总质量为3mg.
①计算所加硫酸镁溶液的质量分数;
②用N表示溶液中离子的数目,不同种离子用离子符号注明[如N (Na')表示钠离子的数目],请建立坐标系,绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图. 查看习题详情和答案>>
氮化铝(AlN)是一种新型无机材料,广泛应用与集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,现用图Ⅰ中的一些装置来进行检验,使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O=NaAlO2+NH3↑,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
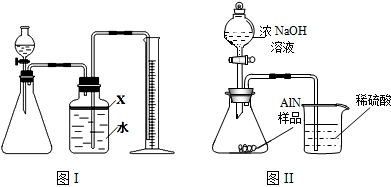
(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为 .
(2)本试验中检查装置气密性的方法是 .
(3)广口瓶中的试剂X可选用 (填选项的标号).A 汽油 B 酒精 C 植物油 D CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将 (填偏大、偏小或不变).
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是 .
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为 (AlN的相对分子质量为41,每22、4L氨气质量为17g).
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行? (填入“可行”、“不可行”).原因是 ,改进的方法为 .
(8)在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液,然后边搅拌边逐滴向其中加入硫酸镁溶液,至溶液的红色完全褪去时,滤去沉淀,称得剩余溶液总质量为3mg.
①计算所加硫酸镁溶液的质量分数;(3分)
②用N表示溶液中离子的数目,不同种离子用离子符号注明[如N (Na')表示钠离子的数目],请建立坐标系,绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图.(3分) 查看习题详情和答案>>

(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为
(2)本试验中检查装置气密性的方法是
(3)广口瓶中的试剂X可选用
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
(8)在mg 20%的氢氧化钠溶液中滴加2~3滴酚酞试液,然后边搅拌边逐滴向其中加入硫酸镁溶液,至溶液的红色完全褪去时,滤去沉淀,称得剩余溶液总质量为3mg.
①计算所加硫酸镁溶液的质量分数;(3分)
②用N表示溶液中离子的数目,不同种离子用离子符号注明[如N (Na')表示钠离子的数目],请建立坐标系,绘制上述滴加过程中各种离子的数目随溶液的不断加入而变化的关系图.(3分) 查看习题详情和答案>>
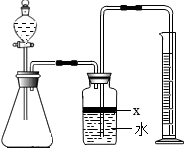 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.【实验目的】测定样品中的氮化铝的质量分数.
【实验原理】AlN+NaOH+H2O=NaAlO2+NH3↑、Al2O3+2NaOH=2NaAlO2+H2O
【实验装置】
【实验步骤】有关操作为:a.往锥形瓶中放入适量的AlN样品:b.从分液漏斗往锥形瓶中加入过量的NaOH浓溶液(不考虑氨气在NaOH浓溶液中的溶解);c.检验装置的气密性;d.测定收集到水的体积.正确的操作顺序为
【交流与讨论】
(1)本实验中检查装置气密性的方法是
(2)广口瓶中试剂x的作用是
(3)小李认为广口瓶中液体没有装满,对氨气体积的测量会产生影响.你对他的观点有何评价?
(4)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
(5)小李同学查阅资料得知实验条件下收集到的气体密度为0.68g/L,若实验中所用量筒规格为500mL,则从理论上分析参加反应的AlN质量的最大值为
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,现用图Ⅰ中的一些装置来进行检验,使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O=NaAlO2+NH3↑,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)已知:NH3非常容易溶于水,氧化铝易溶于NaOH溶液.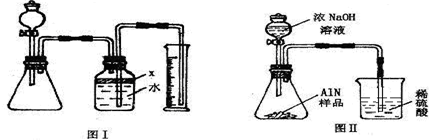
(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为
(2)本试验中检查装置气密性的方法是
(3)广口瓶中的试剂X可选用
A 酒精 B 植物油
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
%
%(AlN的相对分子质量为41,每22.4L氨气质量为17g).
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
查看习题详情和答案>>

(1)实验有关操作为:a、往锥形瓶中放入适量的AlN样品:b、从分液漏斗往锥形瓶中加入过量的浓NaOH;c、检验装置的气密性;d、测定收集到水的体积.正确的操作顺序为
cabd
cabd
.(2)本试验中检查装置气密性的方法是
关闭分液漏斗开关,将导管一端浸入水中,用手紧握锥形瓶外壁,如果导管口有气泡冒出,说明气密性良好,否则装置漏气.
关闭分液漏斗开关,将导管一端浸入水中,用手紧握锥形瓶外壁,如果导管口有气泡冒出,说明气密性良好,否则装置漏气.
.(3)广口瓶中的试剂X可选用
B
B
(填选项的标号).A 酒精 B 植物油
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将
不变
不变
(填偏大、偏小或不变).(5)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是
碳
碳
.(6)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为
| 4100a |
| 22.4w |
| 4100a |
| 22.4w |
(7)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?
不可行
不可行
(填入“可行”、“不可行”).原因是会使液体沿着导管倒吸入锥形瓶内
会使液体沿着导管倒吸入锥形瓶内
,改进的方法为在导管末端接一倒置的漏斗
在导管末端接一倒置的漏斗
.