摘要:14.价电子数为1的X原子和价电子数为6的Y原子.它们形成化合物的化学式可能是 A.XY2 B.XY C.X2Y D.X2Y3
网址:http://m.1010jiajiao.com/timu3_id_153048[举报]
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)W元素在周期表中的位置为
(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于
(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44kJ热量,则该反应的热化学方程式为
(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下D与NaOH溶液反应的离子方程式
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
(5 )X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为
查看习题详情和答案>>
(1)W元素在周期表中的位置为
第三周期第VⅠA族
第三周期第VⅠA族
;写出Y元素原子的价电子排布式:2S22P3
2S22P3
;(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于
极性
极性
(填“极性”、“非极性”)分子.(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44kJ热量,则该反应的热化学方程式为
N2(g)+3H2(g) 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol
 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/molN2(g)+3H2(g) 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol
. 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下D与NaOH溶液反应的离子方程式
NH4++OH-
H2O+NH3↑
| ||
NH4++OH-
H2O+NH3↑
.
| ||
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
SO32-+Cl2+H2O═SO42-+2Cl-+2H+
SO32-+Cl2+H2O═SO42-+2Cl-+2H+
.(5 )X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为
H2+2OH--2e-═2H2O
H2+2OH--2e-═2H2O
.原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)X元素是
(2)X与Y 形成化合物的电子式为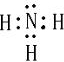
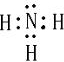 ,X与W组成的化合物中存在
,X与W组成的化合物中存在
(3)写出实验室制备YX3的化学方程式:
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.则A的名称是
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶水.对化合物B进行如下实验:
a. 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体.过一段时间白色沉淀变为灰绿色,最终变为红褐色;b. 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解则B的化学式为
查看习题详情和答案>>
(1)X元素是
氢
氢
(填名称),W在周期表中的位置第三周期第ⅥA族
第三周期第ⅥA族
.(2)X与Y 形成化合物的电子式为
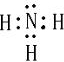
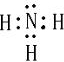
共价
共价
键(填“离子”“共价”).(3)写出实验室制备YX3的化学方程式:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.则A的名称是
硫酸铵
硫酸铵
.(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶水.对化合物B进行如下实验:
a. 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体.过一段时间白色沉淀变为灰绿色,最终变为红褐色;b. 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解则B的化学式为
(NH4)2Fe(SO4)2?6H2O
(NH4)2Fe(SO4)2?6H2O
.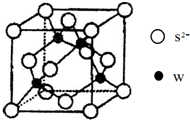 原子序数小于36的X、Y、Z、W四种元素,其中X原子基态时2p原子轨道上有3个未成对电子,Y原子基态时最外层电子数是其内层电子数的3倍,Z元素的最高价氧化物的水化物的酸性最强,W的原子序数为30.
原子序数小于36的X、Y、Z、W四种元素,其中X原子基态时2p原子轨道上有3个未成对电子,Y原子基态时最外层电子数是其内层电子数的3倍,Z元素的最高价氧化物的水化物的酸性最强,W的原子序数为30.(1)元素W的电子排布式为
(2)X、Y与氢元素形成的化合物XH2-YH中采用sp3杂化的原子有
(3)ZO4-离子的空间构型为
(4)元素W的一种硫化物晶体的晶胞结构如右上图所示,该硫化物的化学式是
原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式 ;其中含有的化学键是
(2)X、Z、W三种元素的最高氧化物对应的水化物酸性最强的是(填写化学式):
;
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是(填写化学式);
;
(4)与Z上下相邻的同主族元素M、N,原子电子层数M>Z>N,三种元素氢化物沸点由大到小的顺序是(填写化学式) > >
(5)元素Y的单质在一定条件下,能与氢气化合生成一种固态氢化物YH,熔点为800℃。
①YH晶体类型是
②YH能与水反应放氢气,写出化学方程式
③若将1molYH和1molAl混合加入足量水中,放出气体的体积是(标准状况下) L。
查看习题详情和答案>>