网址:http://m.1010jiajiao.com/timu3_id_113146[举报]
①蒸馏水和食盐水
②氧气和二氧化碳
③硬水和软水
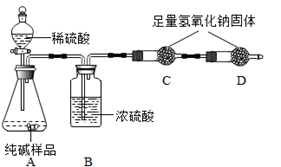
某品牌纯碱中含有少量氯化钠。某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数)。(一)甲组同学设计如图所示实验:
【实验步骤】
①组装好如图仪器,并检查 ;
②称取13.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量;
⑥计算出样品中碳酸钠的质量分数。
【实验分析】
(1)A装置中反应的化学方程式为 。
(2)B装置的作用是 。
(3)如果没有B装置则所测样品中碳酸钠的质量分数 。(填偏大、偏小、不变)
(4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是 。
(5)称得纯碱样品的质量为13.0g,实验前、后C装置(包含药品)的质量分别为61.2g和65.6g,则该纯碱样品的纯度为 %(精确到0.1%)。
(二)乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:
(1)判断加入氯化钡溶液是否过量的合适方法是 ,然后观察现象判断。
A.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量;
B.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量。
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观
察现象判断。
A.氯化钡溶液 B.稀硫酸 C.硝酸银溶液 D.稀盐酸
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为 %(精确到0.1%)。
【实验反思】
甲乙两组同学所测该品牌中碳酸钠的质量分数,你认为 组(填“甲”或“乙”)更准确,另一组存在较大偏差的原因可能是 。
【实验步骤】
①组装好如图仪器,并检查 ;
②称取13.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量;
⑥计算出样品中碳酸钠的质量分数。
【实验分析】
(1)A装置中反应的化学方程式为 。
(2)B装置的作用是 。
(3)如果没有B装置则所测样品中碳酸钠的质量分数 。(填偏大、偏小、不变)
(4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是 。
(5)称得纯碱样品的质量为13.0g,实验前、后C装置(包含药品)的质量分别为61.2g和65.6g,则该纯碱样品的纯度为 %(精确到0.1%)。
(二)乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:
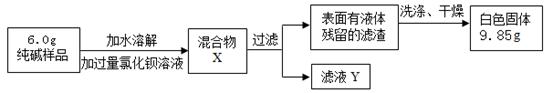
(1)判断加入氯化钡溶液是否过量的合适方法是 ,然后观察现象判断。
A.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量;
B.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量。
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观
察现象判断。
A.氯化钡溶液 B.稀硫酸 C.硝酸银溶液 D.稀盐酸
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为 %(精确到0.1%)。
【实验反思】
甲乙两组同学所测该品牌中碳酸钠的质量分数,你认为 组(填“甲”或“乙”)更准确,另一组存在较大偏差的原因可能是 。
(1)利用吸附、沉淀、过滤和蒸馏等方法可净化水,其中能降低水的硬度的是
(2)小雯采用区别纯水和硬水的方法是:分别取样于蒸发皿中,加热蒸干,有固体析出的是硬水.请你设计另一种方法(简述步骤、现象和结论):
(3)小雯在做实验时,发现硬水在蒸发的过程中,产生了少量气体.
提出猜想:产生的气体可能是二氧化碳;
设计实验:①将生成的气体通入
反馈与应用:通过上述实验得到启发,在家里可用
步骤Ⅰ:将这四种白色固体分别编号为A、B、C、D;
步骤Ⅱ:取少量上述四种白色固体样品分别放入四支试管中,加入足量蒸馏水,振荡,固体全部溶解,且C溶液呈蓝色,则C是______(写化学式,下同);
步骤Ⅲ:取少量A、B、D的溶液分别放入三支试管中,向三种溶液中各加入适量C溶液,装有B溶液的试管中产生蓝色沉淀,则B是______,该反应的化学方程式为______;装有A溶液和D溶液的试管中均有白色沉淀产生;
步骤Ⅳ:为进一步区分A和D,另用两支试管分别取少量A溶液和D溶液,加入适量______溶液,若装有A溶液的试管中产生白色沉淀,则A是______.