摘要:27.实验室制取Cl2的反应为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O.若制得标准状况下的Cl2 4.48L.则被氧化的HCl的物质的量为 mol.转移电子的物质的量为 mol. 28.某烯烃与氢气的加成产物为:CH3 - CH - CH3.该产物的名称是 CH3 ,该烯烃的分子式为 .结构简式为 .
网址:http://m.1010jiajiao.com/timu3_id_103198[举报]
实验室制下列三种气体
A.O2:2KClO3
2KCl+3O2↑
B.CO2:
C.Cl2:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体.
(1)写出制CO2的反应方程式.
(2)有下列三种制气装置(如图甲)和两种集气装置(如图乙)
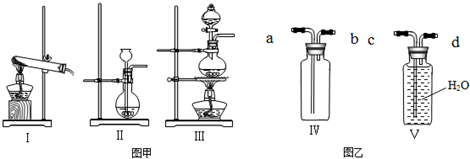
①制取CO2应选取的装置是 ,应选用Ⅲ装置制取的气体是 ;
②用Ⅳ装置收集Cl2应从 口进气,上述三种气体中,能用Ⅴ装置收集的气体有 ,应从 口进气.
(3)A中制O2后,从剩余固体中分离出MnO2的操作有 (不需烘干),所用到的玻璃仪器有 .
(4)用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为 g,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有(至少两点)
(5)将8g KClO3与1g MnO2混合加热制O2,充分反应后冷却,称得试管内剩余固体质量为4.2g,
①请用两种方法求生成KCl的质量
②计算结果表明,题目数据有问题,要使该题数据合理,可将KClO3质量由8g改为a g,则a的取值范围是 .
查看习题详情和答案>>
A.O2:2KClO3
| ||
B.CO2:
C.Cl2:MnO2+4HCl(浓)
| ||
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体.
(1)写出制CO2的反应方程式.
(2)有下列三种制气装置(如图甲)和两种集气装置(如图乙)

①制取CO2应选取的装置是
②用Ⅳ装置收集Cl2应从
(3)A中制O2后,从剩余固体中分离出MnO2的操作有
(4)用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为
(5)将8g KClO3与1g MnO2混合加热制O2,充分反应后冷却,称得试管内剩余固体质量为4.2g,
①请用两种方法求生成KCl的质量
②计算结果表明,题目数据有问题,要使该题数据合理,可将KClO3质量由8g改为a g,则a的取值范围是
实验室制下列三种气体
A.O2:2KClO3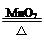 2KCl+3O2↑
2KCl+3O2↑
B.CO2:
C.Cl2:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
写出制CO2的反应方程式
有下列三种制气装置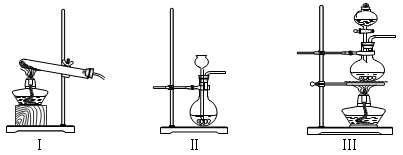
两种集气装置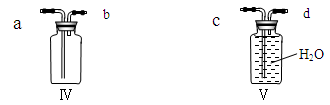
制取CO2应选取的发生装置是 ,应选用Ⅲ装置制取的气体是 ;
用Ⅳ装置收集Cl2应从 口进气,上述三种气体中,能用Ⅴ装置收集的气体有 ,应从 口进气。
A中制O2后,从剩余固体中分离出MnO2的操作有 (不需烘干),所用到的玻璃仪器有 。
用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为 g,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有
, (任写两个)
实验室制下列三种气体
A.O2:2KClO3 2KCl+3O2↑
2KCl+3O2↑
B.CO2:
C.Cl2:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
写出制CO2的反应方程式
有下列三种制气装置

两种集气装置

制取CO2应选取的发生装置是 ,应选用Ⅲ装置制取的气体是 ;
用Ⅳ装置收集Cl2应从 口进气,上述三种气体中,能用Ⅴ装置收集的气体有 ,应从 口进气。
A中制O2后,从剩余固体中分离出MnO2的操作有 (不需烘干),所用到的玻璃仪器有 。
用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为 g,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有
, (任写两个)
A.O2:2KClO3
 2KCl+3O2↑
2KCl+3O2↑B.CO2:
C.Cl2:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O说明:Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
写出制CO2的反应方程式
有下列三种制气装置

两种集气装置

制取CO2应选取的发生装置是 ,应选用Ⅲ装置制取的气体是 ;
用Ⅳ装置收集Cl2应从 口进气,上述三种气体中,能用Ⅴ装置收集的气体有 ,应从 口进气。
A中制O2后,从剩余固体中分离出MnO2的操作有 (不需烘干),所用到的玻璃仪器有 。
用100g 36.5%的浓盐酸与足量MnO2混合加热,理论上能制得Cl2的质量为 g,而实际收集到的Cl2质量远远小于这个数值,若操作正确,装置不漏气,则可能的原因有
, (任写两个)
 MnCl2+2X+Cl2↑,其中X的化学式为
MnCl2+2X+Cl2↑,其中X的化学式为 MnCl2+2X+Cl2↑,其中X的化学式为
MnCl2+2X+Cl2↑,其中X的化学式为