马鞍山市2008年市竞赛练习第一册第一章A卷
一、选择题(每题只有1个选项符合题意):
1、下列做法正确的是( )
A、用手拿药品
B、用灯冒盖灭酒精灯
C、为节约药品,用剩后的药品放回原瓶
D、将吸有溶液的滴管平放于桌面
2、实验室里进行过滤和蒸发实验时,都要用到的仪器是( )
A、烧杯 B、玻璃棒 C、蒸发皿 D、酒精灯
3、实验室进行NaCl溶液蒸发实验时,一般有以下操作:①放置酒精灯,②固定铁圈位置,③放置蒸发皿,④加热搅拌,⑤停止加热,利用余热蒸干。其正确的操作步骤为( )
A、②③④⑤① B、①②③④⑤ C、②③①④⑤ D、②①③④⑤
4、通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
A、NaNO3 NaOH B、CuO MnO2
C、KCl MnO2 D、CuSO4 NaOH
5、下列所用除杂试剂(或方法)不正确的是(括号内为杂质)( )
A、CaO(CaCO3)加热 B、CO2(CO)用O2
C、H2(HCl)用NaOH溶液 D、FeSO4(CuSO4)用Fe
6、下列实验操作错误的是( )
A、分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C、过滤时,玻璃棒在引流过程中应轻靠在三层滤纸一边
D、称量时,称量物放在纸上,置于左盘,砝码放在右盘
7、下列仪器常用于物质分离的有( )
①漏斗,②容量瓶,③烧杯,④分液漏斗,⑤天平,⑥量筒,⑦胶头滴管,⑧蒸馏烧瓶。
A、①④⑥ B、②③⑧ C、⑤⑥⑦ D、①④⑧
8、用四氯化碳萃取饱和碘水中的碘,下列说法不正确的是( )
A、实验使用的主要仪器是分液漏斗
B、碘在四氯化碳中的溶解度比在水中的溶解度大
C、碘的四氯化碳溶液呈紫色
D、分液时,水从分液漏斗的下口流出,碘的四氯化碳溶液从上口倒出
9、下列有关制取蒸馏水的装置和操作的说法中,不正确的是( )
A、温度计的水银球应插入蒸馏烧瓶内的自来水中
B、冷凝管内水的流向是下进上出
C、实验中需在自来水中加几片碎瓷片
D、蒸馏烧瓶底部必须垫石棉网
10、下列溶液中的Cl-浓度与50mL1mol/LAlCl3溶液中Cl-浓度相等的是( )
A 150mL1mol/LNaCl B 150mL3mol/LKCl
C 75mL2mol/LNH4Cl D 50mL1mol/LCuCl2
11、下列实验合理的是( )
A、用托盘天平称取12.6gMnO2粉末
B、用10mL量筒量取8.76mL稀硫酸
C、用100mL烧杯量取8.23mL蒸馏水
D、用体温表测量沸水的温度为
12、在下列各组物质中,分子数相同的一组是( )
A、
B、
C、标准状况下22.4L水和lmol氧气
D、 0.2mol氢气和2.
13、同温同压下,相同体积的下列气体中,质量最大的是( )
A、CH4
B、NH
14、Na2SO4和A12(SO4)3的混合溶液中,Al3+的浓度为0.2mol/L,SO42-的浓度为0.4mol/L,溶液中Na+的物质的量浓度是( )
A、0.1mol/L B、0.2mol/L C、0.3mol/L D、0.4mol/L
15、跟44gCO2的物质的量相等的是( )
A、1.8gH2O B、6.02×1023个C12分子
C、0.5molH2分子 D、标准状况下 2.24LO2
16、下列溶液中,NO3-的物质的量浓度最大的是( )
A、500mL l mo1/L硝酸钾溶液 B、250mL 1mol/L硝酸镁溶液
C、500mL 0.5mol/L硝酸钡溶液 D、250ml 0.5mol/L硝酸铁溶液
17、等量的四份盐酸分别与足量的下列物质完全反应后,所得溶液浓度最小的是( )
A、Mg B、MgO C、MgCO3 D、Mg(OH)2
18、一个O2分子的质量为( )
A、 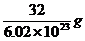 D、
D、 
19、下列叙述中正确的是( )
A、 常温常压下,32gO3含氧原子数为2NA
B、 0.5LCaCl2溶液中含有Ca2+数为0.5NA
C、 0.1mol/LMgCl2溶液中含Cl-数为0.2NA
D、 1molH的质量与NA个氢气分子的质量相等
20、下列说法正确的是( )
A、 物质的量就是物质的质量
B 、物质的摩尔质量就是其相对分子质量
C 、标准状况下,气体的摩尔体积约为
D 、阿伏加德罗常数约为6.02×1023
二、填空题:
21、用食盐固体配制一定物质的量浓度的氯化钠溶液,常用的仪器有 。实验室常用的容量瓶有 等几种规格, 配制一定物质的量浓度的溶液的实验步骤主要有 、 、 、转移、 、摇均、装入试剂瓶、贴标签等。若在配制操作中有以下行为,将会对配制结果造成什么样的影响(填偏大、偏小、不一定或无影响)?
(1)、称量时,物体与砝码的位置颠倒 。
(2)、容量瓶内壁存有水珠 。
(3)、定容时仰视读数 。
(4)、未用蒸馏水洗涤烧杯内壁 。
(5)、溶质溶解后,没有恢复至室温转移 。
(6)、用量筒量取液体时,俯视读数,使所读溶液体积偏小 。
(7)、天平的砝码沾有其他物质或已生锈 。
(8)、用胶头滴管向容量瓶用加水至刻度线后,反复摇匀后发现液面低于刻度线,再加水至刻度线 。
22、用托盘天平称取一定量药品的主要步骤有以下几步,①在左盘上放药品使天平平衡,②调零,③砝码放回砝码盒,④在天平两边托盘上各放一张大小相同的同种纸,⑤按所须称量的药品数量在右盘上放相应数量的砝码并移动游码,⑥游码移回零刻度处,正确的步骤是 。第⑤步操作中放砝码及移动游码的先后顺序为 ,用托盘天平称量NaOH时应注意 。
23、粗盐中除含有不溶性的泥沙外(泥沙不与一般的试剂及常见的酸碱反应),还含有可溶性的杂质有 ,实验室常用①BaCl2、②Na2CO3、③NaOH、④稀HCl等试剂除去可溶性的杂质,并配以适当的操作即可用这样的粗盐经提纯可获得纯NaCl固体。
(1)实验时除杂试剂的加入顺序为 ;
(2)确定过滤操作在实验中的先后顺序的理由是 ;
(3)加入稀HCl的目的是 ;
(4)判断所加的BaCl2已经过量的方法是 ;
(5)加入Na2CO3的目的是 ,确定加入Na2CO3在实验中的先后顺序的理由是 ;
(6)此实验中,过滤时,对过滤出的固体可以洗涤,也可以不洗涤。若选择洗涤,其理由是 ,若选择不洗涤,其理由是 ;
(7)为检验提纯后的食盐中是否仍含有Ba2+的杂质,其检验方法是 ;
(8)若称取粗盐m1g,最后得精盐m2g,则该粗盐的纯度为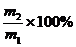 。试评价这一计算结果的正确性。
。试评价这一计算结果的正确性。
24、(1)用已准确称量的1.06gNa2CO3固体配制0.100mol/LNa2CO3溶液100mL,所需要的仪器为 ;
(2)除去NaNO3固体中混有的少量KNO3,所进行的操作依次为: 、蒸发结晶、 。
(3)除去KCl溶液中的SO42-离子,依次加入的试剂是 。
25、选择合适的方法分离或提纯下列物质:
分离或提纯的物质
分离或提纯的方法
分离BaSO4和BaCl2固体
分离食盐和碘
从碘水中提取碘单质
用自来水制取蒸馏水
从Na2SO4溶液中获得Na2SO4固体
26、用木炭还原氧化铜的实验进行一段时间后,停止加热,试管中仍然有黑色固体。为确定反应后黑色固体的成分,请你提出确定黑色固体的所有可能猜想,并设计简单、易行的实验方案,证明你的猜想。
猜想黑色固体是
实 验 操 作
现 象
(1)
(2)
(3)
27、若从H2SO4、Na2CO3、Na2SO4、NaCl、NaNO3、Cu(NO3)2、HNO3七种溶液中取出其中的两种,进行混合及有关实验,所观察到的现象记录如下表。试根据各步实验和现象先进行分步推断,再推断所取的两种溶液的可能组合。
步骤
实 验 操 作
实 验 现 象
推 断(或结论)
(1)
将取出的两种溶液混合
混合溶液无色、澄清
混合液中肯定不含Cu(NO3)2
无明显现象
混合液肯定不是下列组合:
(2)
用PH试纸测定混合液的PH
测定结果:PH=2
(3)
向混合液中滴入足量Ba(NO3)2溶液
有白色沉淀出现
(4)
向上述过滤所得滤液中滴加AgNO3溶液
无明显现象
混合溶液的可能组合(写出溶质的化学式,有几组写几组)
①
②
③
④
28、填写下列表格:
物质
分子数
质量/g
物质的量/mol
摩尔质量/g•mol-1
N2
14
H2SO4
3.01×1022
H2O
0.5
29、现有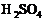 和
和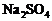 的混合溶液,其中
的混合溶液,其中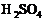 的物质的量浓度
的物质的量浓度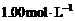 ,
,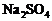 的物质的量浓度为
的物质的量浓度为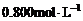 。欲使
。欲使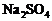 的浓度变为
的浓度变为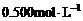 ,应将溶液稀释至
毫升,若要同时使
,应将溶液稀释至
毫升,若要同时使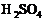 的浓度变为2.00mol?L-1应向原溶液中加入98%(ρ=
的浓度变为2.00mol?L-1应向原溶液中加入98%(ρ=
三、计算题:
30、某温度下,22%的NaNO3溶液150mL,加