2009年广安市高中阶段教育学校招生考试
化学
(满分90分,考试时间90分钟)
可能用到的相对原子质量:H~
一、选择题(本题包括18小题,每小题2分,共36分。每小题只有一个选项符合题意)
1.物质的性质决定物质的用途。下列关于氢气用途的叙述中,只体现物理性质的是 ( )
A.制备金属材料 B.充灌探空气球
C.做火箭高能燃料 D.制备盐酸
2.下面所述的各物质中属于纯净物的是 ( )
A.纯净的空气 B.“农夫山泉”矿泉水
C.用KMnO4制取O2后剩余的固体 D.冰水混合物
3.下列叙述正确的是 ( )
A.物质都是由分子和原子构成的
B.分子能够再分,原子不能再分
C.化学反应中分子再分为原子,原子不变
D.分子都是由多个原子构成的
4.元素周期表是学习和研究化学的重要工具。下图是周期表中铁元素一些信息,下列说法中错误的是 ( )
26 Fe
铁
55.85
A.铁的原子序数是26
B.铁原子核中的质子数是26
C.铁的元素符号是Fe
D.一个铁原子的质量是55.85 9
5.分类是学好化学的基本方法,下列各组物质的分类正确的是 ( )
A.金属单质 Mg Ag S B.酸 HNO3 HCl H2CO3
C.氧化物 Cl2O7 N2O4 KClO3 D.碱 NaOH Ba(OH)2 K2CO3
6.绿色化学即环境友好化学,其理想状态就是参加反应的原子全部转化为要制备的物质。下列化学反应一定符合绿色化学理念的是 ( )
A.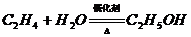
B.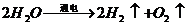
C.HCl+AgNO3==AgCl↓+ HNO3
D.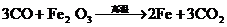
7.同种元素形成的不同种单质互为同素异形体,下列各组物质不属同素异形体的是 ( )
A.金刚石与C60 B.O2与O3
C.白磷与红磷 D.纯碱与火碱
8.NO有毒,在空气中极易与氧气反应生成NO2,造成空气污染。但少量的NO在人体内具有扩张血管、增强记忆的功能,被誉为“明星分子”。通常状况下,NO密度比空气略大,难溶于水。则实验室收集NO的装置是 ( )
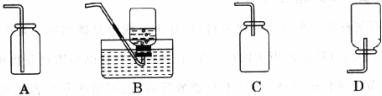
9.我国已正式实施“限塑令”以控制白色污染。国家倡导大家使用无纺布袋。生产无纺布袋的主要原料为:聚乙烯、聚丙烯、聚酯和粘胶等。下列说法不正确的是 ( )
A.大部分塑料制品在自然环境中很难降解
B.使用无纺布袋有利于减少“白色污染”
C.生产无纺布原料与生产棉布的原料相同,都是天然纤维
D.聚乙烯、聚丙烯、聚酯、粘胶都属于合成材料
10.具备基本的化学实验技能是进行科学探究的基础和保证。下列操作正确的是
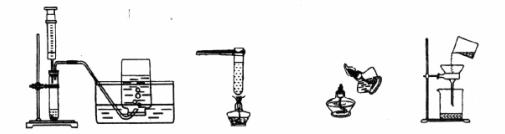
A.用过氧化氢制取氧气 B.加热液体 C.点燃酒精灯 D.过滤
11.研究问题的方法很多。下列研究问题的方法不合理的是 ( )
A.采用向冷而干燥的玻片上“哈气”,证明呼出的气体中含有较多的水蒸气
B.采用加入肥皂水,区别硬水和软水
C.采用调查、走访,寻找河水的污染源头
D.采用做灯火试验,检查家里液化石油气是否泄漏
12.美籍华裔科学家钱永健因研究绿色荧光蛋白方面的突出贡献而获2008年度诺贝尔化学奖。下列关于蛋白质的说法错误的是 ( )
A.蛋白质是构成细胞的基本物质
B.人体通过食物获得的蛋白质,在胃肠里与水反应生成氨基酸
C.荧光蛋白属高分子化合物
D.酶是一类重要蛋白质,是生物催化剂,一种酶能催化多个反应
13.铁磁性纳米材料Fe3O4的一种制备方法为FeCl2+2FeCl3+8NaOH===Fe3O4+8X+4H2O,则产物X的化学式是 ( )
A.NaClO B.NaClO
14.下列做法正确的是 ( )
A.因浓盐酸具有挥发性,所以浓盐酸必须密封保存
B.用盐酸除去Fe粉中的Cu粉
C.人体缺钙会导致佝偻病,为了补钙,需要长期饮用硬水
D.胃酸过多的病人可吃NaOH,以减少胃酸
15.下列各组物质能在无色溶液中大量共存的是 ( )
A.CuSO4 NaOH HCl B.FeSO4 BaCl2 AgNO3
C.NaCl KNO3 H2SO4 D.Na2CO3 Ca(OH)2 HNO3
16.
A.-2 B.
17.下列归纳整理与解释正确的是 ( )
A.现象与解释
B.物质鉴别
丹桂飘香――分子间存在较大的间隔
鉴别NH4NO3、NaOH、NaCl三种固体――水
C.生活常识
D.环境保护
煤炉取暖防中毒――室内放一盆水
减少酸雨污染――不使用煤作燃料
18.向一定质量的盐酸中加入足量的铁粉,下图所示反应中各变化错误的是( )
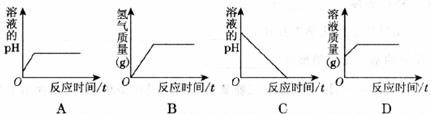
二、我会填写(本大题共29分)
19.(6分)(1)用数字或符号填空:①两个氮原子__________ ;②正2价的钙元素__________。
(2)在氮气、甲烷、一氧化碳、熟石灰、纯碱中选择适当物质,用化学式填空:
①属于有机物的是__________;
②常用来改良酸性土壤的物质是__________;
③通常用于食品包装的气体是__________;
④
20.(3分)下列四种粒子结构示意图,请据图回答问题:
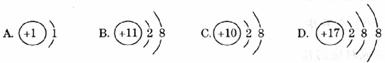
(1)上述粒子中,属于阳离子的是_________ (填该离子的符号);
(2)D粒子所属元素的名称是_________;
(3)上述A、D两种元素组成化合物的化学式为_________
21.(2分)下图为A、B两种物质的溶解度曲线,根据曲线回答下列问题:
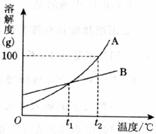
(1) t
(2)t
22.(5分)在一密闭容器中。有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质质量如下表:
物质
甲
乙
丙
丁
反应前质量/g
3
5
20
4
反应后质量/g
待测
14
3
12
请分析该表后,回答下列问题:
(1)反应后甲的质量为________g,反应中甲物质的作用可能是________。
(2)该反应中生成物的质量比为________。
(3)写出符合该反应类型的一个化学方程式________________________
23.(6分)A、B、C三种物质之间在一定条件下有如图所示的转化关系。若A为红色单质,B为黑色粉末,C的水溶液为蓝色,试推断:
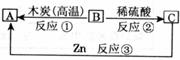
(1)B物质名称________
(2)写出反应③的化学方程式________
该反应的基本反应类型是________。
三、我会计算(本大题共8分)
25.(8分)石灰石是一种重要的建筑材料,其主要成分是碳酸钙。现取80.
实验分组
甲
乙
丙
丁
石灰石样品质量/g
20.0
20.0
20.0
20.0
加入盐酸质量/g
30.0
60.0
90.0
120.0
生成CO2质量/g
2.2
4.4
6.6
6.6
(1)___________组同学加入的盐酸恰好完全反应。
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)求丙组同学实验后溶液中溶质的质量分数(计算结果保留一位小数)。
四、我来探究(本大题共17分)
26.(5分)如图所示装置有多种用途。按要求回答下列问题:

(1)洗气:除去H2中的水蒸气,装置内盛装的液体物质是_______。
(2)集气:用排空气法收集O2时,气体从装置的_______端通入。
(3)检验:证明CO中含CO2,装置内盛装的液体物质是_______。
(4)测量气体体积:瓶内先装满水,气体从_______端通入,还需要用到的一种仪器是_______ (填写仪器名称)。
27.(12分)同学们,中考之旅即将结束,暑假生活又该怎样安排呢?那请你参加“红色之旅”夏令营活动吧。
(1)当前,甲型H1Nl病毒正值敏感传染期,旅途中为预防甲型H1Nl等各种疾病的传染,下列措施错误的是___________
A.使用消毒液对公共场所进行经常性的消毒处理
B.养成良好的卫生习惯,若发热应及时去医院就诊
C.居室要勤通风换气.吃熟食,尽量少去人流聚集的地方
D.要与世隔绝,不参加任何活动,以免与人接触发生传染
(2)来到“小平故居”,“故居”墙壁上悬挂的铁犁、铁耙、铁锄等农具上都涂了一层薄薄的油性物质以防止生锈,防锈的原理是________。
(3)同学们来到华蓥山,参观了“双枪老太婆”战斗过的地方后,准备生火野炊。此时有同学说,森林地区不能生火野炊,其原因是________
(4)同学们被安排到指定地点进行野炊,饭后发现搭建灶台的石灰石部分变成了白色块状物质。同学们将此白色物质带回实验室进行探究,以确定其组成。
[提出问题]白色块状是由哪些成分组成的?
[作出猜想]假设1:只有碳酸钙
假设2:只有氧化钙
假设3:是碳酸钙和氧化钙的混合物
[实验证明]
第一步:将白色物质溶于足量的水中,过滤。
第二步:取滤液,向滤液中滴加酚酞试液,溶液显红色,则假设________不成立;滤液的pH ________7(填“>”“<”或“一”)。
第三步:取滤渣,滴加稀盐酸,有大量气泡产生,则假设________不成立。将此处所得气体通人澄清石灰水中,现象是________,
写出此反应的方程式________________________________。
[得出结论]由探究得知假设________成立。