2009年湖北省恩施自治州初中毕业生学业考试
物理、化学试卷
化学部分(满分50分)
 温馨提示:亲爱的同学, 绚丽多彩的化学世界伴你走过三百六十五里路,让你深切感受到化学的无穷魅力――让生活更加美好。请你以“见著而知微,见微而知著”的方法再次探究化学世界。
温馨提示:亲爱的同学, 绚丽多彩的化学世界伴你走过三百六十五里路,让你深切感受到化学的无穷魅力――让生活更加美好。请你以“见著而知微,见微而知著”的方法再次探究化学世界。
可能用到的相对原子质量:H-1 O
一、选择题(每题只有一个正确答案,将正确答案填入下列答题栏中,每题2分,共20分)
1.下列有关生活常识的说法中正确的是
A.废电池应该集中回收处理 B.“白色污染”是指白色物质造成的污染
C.纯净水中不含任何化学物质
D.“绿色食品”是指颜色一定为绿色的食品
2.我国是自然灾害频发的国家,灾害中常有如下现象发生,其中属于化学变化的是
A.冰雪融化 B.房屋倒塌 C.森林失火 D.树枝折断
3.已知某两种物质在光照条件下能发生化学反应,观察其微观示意图(见下图),所得信息正确的是(说明:一种小球代表一种原子)
4.有关三聚氰胺的描述正确的是
A.三聚氰胺的物理性质是:它是一种白色晶体,微溶于水,低毒,高温可分解。
B.三聚氰胺是有机物
C.三聚氰胺是一种高纯度的蛋白质
D.材料中加点的“氮”是指氮分子
5.下列对三聚氰胺的说法正确的是
A.三聚氰胺是由C、N、H三种原子构成 B.三聚氰胺的相对分子质量为
C.三聚氰胺含氮量约为66.7% D.三聚氰胺中C、N元素的质量比为1:2
6.下图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是
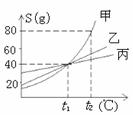
A.t
B.t
C.要使t
D.t
7.下列鉴别物质的方法中,不可行的是
A.用酚酞试液鉴别稀硫酸和Na2SO4 溶液 B.用点燃的方法鉴别羊毛和涤纶
C.用嗅气味的方法鉴别白酒和食醋 D.用水鉴别NaCl和CaCO3固体
8.善于归纳知识,利于培养素质。下面是小青同学对部分化学知识的归纳,其中有错误的一组是
A.化学与健康
B.实验记录
①人体缺铁会引起贫血症
②多吃水果蔬菜利于补充维生素
③用活性炭净水器可净化饮用水
①用10ml量筒量取7.25ml 水
②用pH试纸测得苹果汁的pH为3.2
③用托盘天平称取
C.化学与能源
D.安全常识
①煤、石油、天然气--不可再生的化石燃料
②风能、水能、太阳能--未充分利用的绿色能源
③使用氢能源--可以缓解温室效应,减少酸雨。
①厨房煤气管漏气--关闭阀门并开窗通风
②实验时碰倒酒精灯着火--用湿抹布盖灭
③冬天用煤炉取暖--保证室内通风
9.下图可表示将pH=1的盐酸加入到pH=14的氢氧化钠溶液中恰好完全反应的是
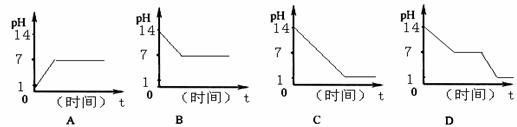
10.现有
选项
A
B
C
D
Ag
Zn
Fe
Mg
金属活动性顺序
强 K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 弱
二、填空题(每空1分,共25分)
11.生活处处有化学。请用下列物质的序号填空:
①浓盐酸 ②烧碱 ③碳酸氢钠 ④生石灰 ⑤硝酸钾
⑴ 常用于金属除锈的是 ; ⑵ 常用于治疗胃酸过多的是 ;
⑶ 可用作化肥的是 ; ⑷ 常用于干燥剂的是 ;
⑸ 属于碱的是 。
12.元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究:
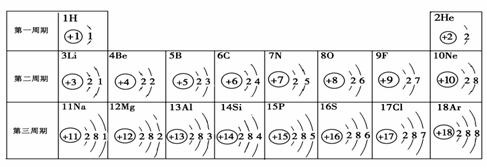
⑴ 第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶ 在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径 变化规律是 _________________________________。
13.镁合金的强度高、机械性能好,其成分镁是制造汽车、飞机、火箭的重要材料,享有“国防金属”的美誉。下图是从海水中提取镁的全过程,请回答下列问题:
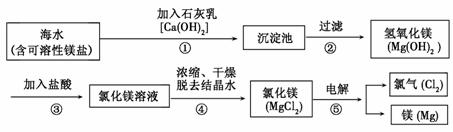
(1)镁合金是 (填“单质”、“化合物”、“混合物” )
(2)下图是镁元素的某种粒子的结构示意图,该图表示 (填粒子符号)。
(3)化学反应前后有元素化合价变化的反应属于氧化还原反应。其中③⑤的反应属于氧化还原反应的是 ,其化学方程式为 ;属于复分解反应的是 ,其化学方程式为 。
14.草酸的化学式为H
【猜想与假设】
第一种:草酸分解产物是CO2和H2 ; 第二种:草酸分解产物是CO2、CO和H2O ;
第三种:草酸分解产物是 CO2和H2O ; 第四种:草酸分解产物是CO2、CO 。
以上猜想,第 种一定不可能,原因是 。
【查阅资料】无水硫酸铜遇水由白色变成蓝色,碱石灰是一种常用的干燥剂。
【实验设计】(图中铁架台略去)甲同学设计了甲装置,乙同学设计了乙装置。
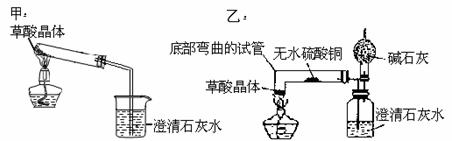
【实验过程】甲同学按甲装置实验,在给草酸晶体加热时,先 ,然后固定在 底部加热,过一会儿观察到澄清石灰水变浑浊;乙同学按乙装置实验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在干燥管的尖嘴处点火能燃烧,乙同学进一步通过实验验证燃烧的气体为CO,他的操作是
,现象是 。
【实验结论】第 种猜想是正确的,请写出草酸受热分解的化学方程式 。
【反思与评价】乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到
三、计算题(5分)
15.在实验室制取氧气时,取MnO2和KClO3的固体混合物
编号
1
2
3
4
加水的质量(g)
10
10
10
10
剩余固体的质量(g)
7.25
4.05
m
3
试求:(1)表中m值为 。
(2)所制得氧气的质量。