2007-2008学年度烟台市莱阳第一学期初三期末考试
化学试卷
注意事项:
1.本试题分为选择题和非选择题两部分,满分l00分,考试时间60分钟.
2.请考生将密封线内的项目填写清楚.
3.本卷可能用到的相对原子质量:C:12 Cl:35.5 N:l4 H:l S:32 O:16
一、选择题(下列各小题均有一个正确答案,本题包括15小题,每小题2分,共30分。)
1.学习化学后,我们懂得世界是物质的,物质是变化的。下列日常生活中的变化属于化学变化的是
A.蜡烛熔化 B.酒精挥发 C.电灯泡通电发光 D.食物腐烂
2.下列家庭中常用的物质中属于纯净物的是
A.自来水 B.白醋 C.蒸馏水 D.白酒
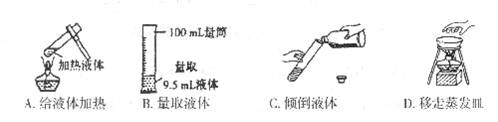
3.在实验室里,下列操作中正确的是
4.印度洋海啸后,使当地的饮用水受到污染。医疗救护人员打算给当地居民提供一些关于饮用水的处理建议,请你帮助判断以下建议不合理的是
A.用明矾使水中悬浮颗粒泥降下来
B.用漂白粉对水进行消毒杀菌
C.通过观察水只要无色透明,就可以放心饮用
D.水在饮用前一定要加热煮沸
5.现有质量分数为10%的某溶液,若使其质量分数增大一倍,可采用的方法是
A.将溶剂蒸发掉一半
B.将溶质质量增大一倍
C.蒸发溶剂的质量为原溶液质量的1/2
D.溶质、溶剂质量同时减少l/2
6.下列操作或现象与分子对应的特性不一致的是
选项
操作或现象
分子的特性
A
给蓝球充气
分子间有间隙
B
100mL酒精和100mL水混合在一起,体积小于200mL
分子是有质量的
C
在花园中可闻到花的香味
分子是运动的
D
加热氧化汞可得到金属和氧气
分子是可以再分的
7.R元素原子的最外层电子数为2,下列关于R原子和R离子的说法正确的是
A.化学性质相同 B.电子层数相同
C.相对原子质量相同 D.最外层电子数相同
8.含磷洗涤剂主要成分为Na5P3Ox,大量使用会造成水污染,环保部门明令禁止生产和使用该洗涤剂。已知该化合物中磷元素为+5价,则化学式中x值的
A.5 B.
9.下列各组物质中,是按单质、化合物、混合物顺序排列的是
A.自来水、氧化镁、液态空气 B.稀有气体、稀硫酸、食盐
C.水银、蒸馏水、石灰水 D.二氧化碳、铁、氢氧化钠溶液
10.实验室制取氧气时,必须满足的条件是
A.必须使用催化剂 B.必须用含氧元素的物质作反应物
C.必须用排水法 D.必须用燃着的木条检验是否集满
11.下列有关原子的说法中正确的是
①原子是化学变化中的最小微粒;②原子不能再分;③原子在化学变化不能再分;④原子中肯定含有质子、中子、电子三种微粒;⑤原子核在化学变化中不发生变化
A.①②③ B.①③④ C.①②⑤ D.①③⑤
12.世界卫生组织将某氧化物RO2列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。实验测得该氧化物中的R与O的质量比为71:64,则RO2的化学式为
A.CO2 B.ClO
13.新装潢的家庭居室存在严重的室内污染,其主要有害成分之一是甲醛化学式(CH2O),它来源于室内装潢所用的油漆、胶合板等材料,长期接触甲醛的人们易痪口、鼻、喉及肺部肿瘤等疾病。下列关于甲醛的说法中正确的是
A.甲醛是一种氧化物
B.甲醛中C、H、O三种元素的质量比为6:l:8
C.甲醛分子中含有氢分子
D.甲醛分子是由一个碳原子和一个水分子构成
14.为了揭开原子内部结构的奥秘,1911年著名物理学家卢瑟福等人做了一个著名的“卢瑟福实验”:用一束带正电的质量比电子大很多的高速运动的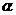 粒子轰击金箔,结果是大多数
粒子轰击金箔,结果是大多数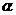 粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,甚至有极少数的
粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,甚至有极少数的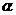 粒子被反弹了回来。通过这一实验现象不能够获得的结论是
粒子被反弹了回来。通过这一实验现象不能够获得的结论是
A.原子核质量较大 B.原子核体积很小
C.核外电子带有负电荷 D.原子核带有正电荷
15.相同质量的CO2和CO两种气体中,所含碳元素的质量比为
A.11:7 B.7:
二、填空题(本题包括6个小题,共36分。)
16.学习化学离不开化学探究活动,其基本环节大体应包括_________、_________、_________、_________、_________。
17.某原子x的相对原子质量为23,该原子的原子核内质子数比中子数少1个,则该原子核内质子数为_________,中子数为_________,核外电子数为_________。
18.学习化学要逐步建立“微粒观”,我们已经学习和接触了以下几种微粒:①分子②原子③离子④原子核⑤质子⑥中子⑦电子。请用其序号恰当地填写在以下空白:
(1)通常是带电的微粒有________,一定带正电的是________,呈电中性的有________;
(2)能构成物质的微粒有_________,化学变化中最小的微粒是_________;
(3)质量最小的微粒是_________,在同一原子中数目相等的微粒是_________.
19.化学实验是学习化学的基本手段,而要进行化学实验,就离不开常用仪器.请选用适当仪器填写下列实验操作所必需的仪器(每空只填一种主要仪器):
(1)取用粉末状固体药品时使用_________;取用块状固体药品时一般使用_________;取用或滴加少量液体药品时使用_________;量取一定体积的液体药品时使用_________。
(2)称量固体药品的质量时使用_________;给药品加热时使用_________。
20.请你各举出一个实例,说明下列有关溶液的叙述是错误的.
(1)溶液一定是无色的;实例:_________溶液不是无色的。
(3)溶液中的溶质一定是固体;实例:_________可做溶质,但不是固体。
(2)均一、稳定的液体都是溶液;实例:_________是液体,但不是溶液。
21.如图所示,用此装置测量空气中氧气的含量,在燃烧匙中加入红磷,红磷与空气中的氧气发生化学反应生成五氧化二磷固体,请按要求填空。
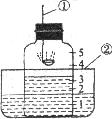
(1)写出标号仪器的名称:①_____________②____________。
(2)在空气中点燃①中的红磷,并迅速插入玻璃罩内,塞紧橡皮塞,此时看到的主要现象是________________________,该变化的文字表达式为________________________.
(3)当红磷燃烧完毕,钟罩冷却到室温后,看到钟罩内水面的变化是____________,出现该现象的原因是:红磷燃烧消耗了空气中气态的____________而生成了固态的____________,从而使钟罩内气体的体积____________ (“增大”“减小”或“不变”),钟罩内气体压强____________ (“大于”、“小于”或“等于”)钟罩外的大气压。
(4)上述实验除以可以得出“氧气约占空气体积____________”的结论外,还可以得出有关氮气的性质结论是____________________________________________________________.
三、简答题(本题包括2个小题。共l0分。)
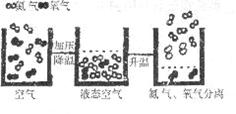
22.氧气是一种化学性质比较活泼的气体,纯净氧气在工业、医疗、航空、航天等方面有着极其广泛的用途,工业上常用分离液态空气法制取氧气。下图是从空气中分离氧气示意图,由此图你可获得的信息有哪些?(至少4条)
23.请写出下列变化的文字表达式,且在相应的物质名称下面写出物质的化学式,在文字表达式后面注明反应类型。
(1)水在直流电作用下发生反应
(2)实验室用双氧水制氧气
(3)光亮铁丝在纯氧中燃烧
四、实验探究题(本题包括2个小题,共l5分。)
24.为监测某厂排放的污水中银离子的含量,需配制
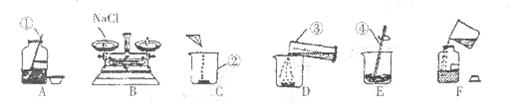
请你帮助解决以下问题:(注:有些空白填“变大”“变小”“不变”)
(1)图示的操作中,___________操作有错误,改正方法是____________________;
(2)若在进行B操作时,砝码与氯化钠的放置位置颠倒(
(3)若其它操作均正确,量取水时仰视读数,则所配溶液的溶质质量分数__________。
(4)若在进行F操作时,有少量溶液洒落,则所配溶液的溶质质量分数__________。
(5)E操作的作用是________________________________________。
25.化学兴趣小组为了研究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如图所示)可能是什么物质,大胆猜想并设计实验进行验证。
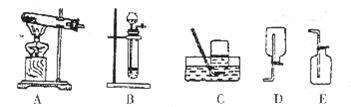
[发现问题]当把黑色粉末与无色溶液混合时即产生气泡。
[查阅资料]初中化学实验室常见的黑色粉末有CuO、MnO2、Fe3O4、铁粉、炭粉等。
[提出假设]黑色粉末是__________,无色溶液是__________。(只写一种假设)
[设计实验]①向盛有少许黑色粉末的试管中加入适量的无色溶液;②检验试管中产生的气体(写出操作方法) ________________________________________。
[实验现象] ______________________________。
[实验结论]①该反应的文字表达式是____________________。
②此气体是____________________,原假设成立。
[讨论]若要制取该气体,应从下图中选择发生反应的装置是__________,收集装置为__________ __________ (填序号)。
五、计算题(本题包括2个小题,共9分。)
26.青少年正处在身体生长发育期,要远离毒品,拒绝香烟。烟草中含有对身体健康危害极大的烟碱(尼古丁),其化学式为C10H4N2,它的相对分子质量为__________,其中碳、氢、氮三种元素的最简质量比为__________。
27.过氧化氢的水溶液俗称双氧水,在放置过程中会缓慢分解。现有一瓶未曾使用过的久置双氧水,瓶上商品标签提供了如下信息:
①H2O2:的质量分数为30%;
②内装溶液质量
③实验测定,其中H2O2的质量分数仅为10%。计算:
(1)若用这瓶双氧水来配制H2O2的质量分数为3%的医用双氧水
(2)这瓶双氧水已分解的过氧化氢的质量计算式为: