2007年聊城市临清初三模拟考试化学试卷
说明:
1.试题由第Ⅰ卷和第Ⅱ卷组成,共12页。第Ⅰ卷为选择题,第Ⅱ卷为非选择题。两卷分别包括物理部分、化学部分、生物部分,共l50分。考试时间为120分钟。
2.答第Ⅰ卷前,请你先将姓名、准考证号、考试科目涂写在答题卡上,考试科目只涂物理,不涂化学和生物。每题选出答案后,都必须用2B.铅笔把答题卡上对应题目的答案标号(ABCD)涂黑,如需改动,必须用橡皮擦干净,再改涂其他答案。
3.试题的第Ⅱ卷分别在物理答卷、化学答卷、生物答卷上作答。考试结束,将答卷、答题卡、试题一并交回。
第Ⅰ卷(选择题 共57分)
相对原子质量:H―1 O一
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意)
12.下列俗语与物质的化学性质无关的是
A.真金不怕火炼 B.百炼方能成钢 C.纸里包不住火 D.玉不啄不成器
13.石油是一种没有固定沸点的油状物,经过气化、冷凝分离后可得到汽油、煤油等产品。由此可以判定石油属于
A.单质 B.化合物 C.混合物 D.纯净物
14.有一瓶失去标签的无色气体,有人记得是二氧化碳,有人说不是,大家争论不休,你认为确证该气体的方法应为
A.讨论 B.调查 C.上网 D.实验
15.蔬菜、水果可以调节新陈代谢、维持身体健康,主要原因是蔬菜、水果中富含人体需要的
A.油脂 B.维生素 C淀粉 D.蛋白质
16.要配制
A.将
B.量取90mL水时,俯视读数
C.为加快溶解,用温度计搅拌
D.将配制好的溶液装入试剂瓶中,盖好瓶盖,贴上标签
17.1911年物理学家卢瑟福等人为探索原子的内部结构进行了下图所示实验:用一束带正电的、质量比电子大得多的高速运动的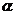 粒子轰击金箔时发现:
粒子轰击金箔时发现:
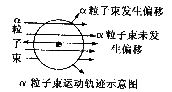
①大多数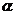 粒子能穿透金箔而不改变原来的运动方向;
粒子能穿透金箔而不改变原来的运动方向;
②一小部分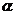 粒子改变了原来的运动方向;
粒子改变了原来的运动方向;
③有极少数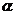 粒子被弹了回来。由此推出关于原子内部结构的一些假设不合理的是
粒子被弹了回来。由此推出关于原子内部结构的一些假设不合理的是
A.原子核体积很小
B.原子是一个实心球体
C.原子核与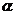 粒子带同种电荷
粒子带同种电荷
D.原子内有相对较大的空间
18.欲将含有盐酸的氯化钙溶液中和至中性,在不用指示剂的条件下,加入的试剂最好是
A.碳酸钙粉末 B.石灰水 C.氢氧化钠溶液 D.碳酸钠溶液
19.小华同学对所学部分化学知识的归纳如图所示,其中有错误的一组是
物质的性质与用途
安全常识
A
N2性质稳定――填充食品袋防腐
乙醇具有可燃性――可用做燃料
CO具有还原性――可冶炼金属
B
假酒中毒――由甲醇引起
瓦斯爆炸――由天然气引起
煤气中毒――由甲烷引起
元素与人体健康
日常生活经验
C
缺铁――易引起贫血
缺钙――易得佝偻病或骨质疏松
缺碘――易得甲状腺肿大
D
去除衣服上的油污――用汽油洗涤
区别白醋和白酒――常用闻气味的方法检验
为使煤燃烧更旺――把煤做成蜂窝状
20.下图是分离与提纯海水的流程:下列有关认识错误的是
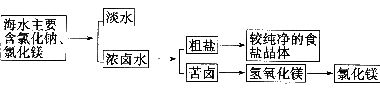
A.常用于淡化海水的方法有蒸馏法、过滤法等
B.将粗盐提纯为较纯净的食盐晶体的操作为:溶解、过滤、蒸发
C.通常在苦卤中加入熟石灰制取氢氧化镁
D.海水中的食盐用途很广,如候德榜利用食盐为原料制得了纯碱
21.下列四个图像,分别对应四种操作过程,其中正确的是
A.向氢氧化钠溶中加入足量水稀释
B.某温度下,向接近饱和的氯化铵溶液中加入氯化铵晶体
C.向氯化铁和盐酸的混合溶液中加入过量氢氧化钠溶液
D.向两份相同体积和相同质量分数的盐酸溶液中分别加入足量的铁粉和镁粉
第Ⅱ卷(非选择题 共93分)
二、(本题包括4小题。共l6分)
1.(6分)有下列几种气体:N2、CO2、CH4、H2、O2,其中能供给呼吸的气体是 ;在空气中体积分数最大的气体是 ;溶于水所得溶液的PH<7的气体是 ;天然气的主要成分是 ,它在空气中燃烧的化学方程式为
2.(4分)目前,化石燃料是人类生产、生活的主要能源。随着全球能源消耗量的增长,化石燃料等不可再生能源将日趋枯竭,世界各国人民的节能意识也日趋增强。科学家也在开发新能源、研制节能产品、提高化学能的转化效率等方面做着积极的努力。请你回答:
(1)有待继续开发、利用的能源有 (请回答三种);
(2)生产、生活中存在着化学能和电能的相互转化。请你分别各举一例:
①由化学能转为电能 ;
②由电能转化为化学能 ;
(3)氢气具有热值高且 的特点,因此被认为是最清洁的能源。
材料一:通常食醋中约含3%―5%的醋酸。醋酸的化学式为CH3COOH,在温度高于l6.
材料二:钙是人体中一种常量元素,人们每日必须摄入一定量的钙。动物的骨头中含有磷酸钙,磷酸钙难溶于水,但能跟酸反应生成可溶性钙盐。
(1)在
(2)生活中能否用铝制品来盛放食醋? ,原因是 。
(3)人们在熬骨头汤时,常常会加入少量的食醋,这样做的理由是
4.(2分)铜和浓硝酸可以发生反应,化学方程式为:
Cu+4HNO3(浓)=Cu(NO3)2+2X↑+2H2O,试回答:
(1)X的化学式是 ;
(2)推断X的化学式的依据是 。
三、(本题包括2小题,共8分)
5.(3分)某学校兴趣小组的同学用干燥管、烧杯、铜网等设计装配了一个实验室制取二氧化碳气体的装置。如图所示,在干燥管内的铜网上应盛放 ;若将铜网换成铁网,可能产生的后果是 ;当在铜网上放上合适的药品,用止水夹夹紧橡皮管时,可观察到的现象为 。
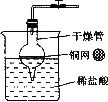
6.(5分)氢氧化钠固体在空气中易变质而含有碳酸钠,某化学研究小组针对这一性质对某氢氧化钠进行以下探究活动:
[确定实验目的]检验氢氧化钠固体中是否含有碳酸钠。
[设计实验方案]方案一:取少量样品加适量蒸馏水配成溶液后,滴入石蕊试液,若观察到液体变蓝色,说明氢氧化钠固体已部分变质。
方案二:取少量样品加适量蒸馏水配成溶液后,滴加足量的澄清的石灰水,若观察到产生白色沉淀,说明氢氧化钠已变质。
[评价与交流]
(1)实验方案评价:上述实验方案中不正确的是 ,因为 ;
(2)方案二中发生反应的化学方程式为 ;
(3)实验方案交流:你也说一说还可以选择 为试剂,同样能达到实验目的。
四、(本题包括1小题,共6分)
7.(6分)工业上用电解水的方法制备氢气和氧气。用电解水的方法分解4.
解:设最多制得氧气的质量为x
2H2O 2H2↑+O2↑
2H2↑+O2↑
36 32
4.
36:32=4.
x=
答:最多制得
小军的解法为:
解:水中氧元素的质量分数:
 ×100%=
×100%=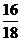 ×100%≈88.9%
×100%≈88.9%
氧的质量为:4.
答:最多制得
请你回答下列问题:
(1)你认为他们的解题思路和方法都正确吗?
(2)13.