摘要:氧的质量为:4.5kg×88.9%=4kg答:最多制得4kg氧气.请你回答下列问题:(1)你认为他们的解题思路和方法都正确吗?
网址:http://m.1010jiajiao.com/timu_id_891568[举报]
请回答下列问题:
(1)加热一定质量的高锰酸钾至完全分解,则生成氧气的质量占高锰酸钾中氧元素的质量分数为 .
(2)小宇同学将16 g高锰酸钾放在试管里加热制取氧气,反应一段时间后,称量试管内剩余固体的质量为14.4 g.
①剩余固体中,含有的物质是 .
②生成二氧化锰的质量(写出计算过程). 查看习题详情和答案>>
(1)加热一定质量的高锰酸钾至完全分解,则生成氧气的质量占高锰酸钾中氧元素的质量分数为
(2)小宇同学将16 g高锰酸钾放在试管里加热制取氧气,反应一段时间后,称量试管内剩余固体的质量为14.4 g.
①剩余固体中,含有的物质是
②生成二氧化锰的质量(写出计算过程). 查看习题详情和答案>>
3.2克某有机物A完全燃烧,生成4.4 克 CO2和3.6克 H20.小李认为A中一定含有碳、氢元素,可能含有氧元素;小张认为A中只含有碳、氧元素,没有氧元素;小王认为一定含有碳、氢、氧三种元素.你认为
查看习题详情和答案>>
小王
小王
的观点是正确的,并通过计算帮助他说服另外两位同学.写出你的计算过程:该有机物中含有C的质量为:4.4×
×100%=1.2g;
该有机物中含有H的质量为:3.6×
×100%=0.4g;
该有机物中含有O的质量为:3.2g-1.2g-0.4g=1.6g
| 12 |
| 44 |
该有机物中含有H的质量为:3.6×
| 2 |
| 18 |
该有机物中含有O的质量为:3.2g-1.2g-0.4g=1.6g
该有机物中含有C的质量为:4.4×
×100%=1.2g;
该有机物中含有H的质量为:3.6×
×100%=0.4g;
该有机物中含有O的质量为:3.2g-1.2g-0.4g=1.6g
.| 12 |
| 44 |
该有机物中含有H的质量为:3.6×
| 2 |
| 18 |
该有机物中含有O的质量为:3.2g-1.2g-0.4g=1.6g
同学在学化学时走向社会和工厂,在实地参观中学到了许多书本上所没有的知识,比如学会了对样品试样的分析;他们从工厂带回一块小矿石,对其化合物的组成进行了实验,装置如下图:
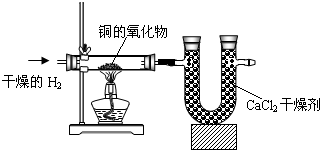
铜的氧化物CaCl2干燥剂实验结果如下:
(玻璃管的质量为80.2g)
试根据实验数据求:
(1)完全反应后生成水的质量为: ;
(2)生成的水中氧的质量为: ;
(3)铜的氧化物中铜的质量为: ;
(4)铜的氧化物中铜和氧的质量比为: ;
(5)计算铜的氧化物中铜、氧原子个数比为 ,确定该氧化物的化学式为 .
查看习题详情和答案>>

铜的氧化物CaCl2干燥剂实验结果如下:
(玻璃管的质量为80.2g)
| 实验前 | 实验后 | |
| 铜的氧化物+玻璃管 | 137.8g | 131.4g |
| 氯化钙+U型管 | 100.8g | 108.0g |
(1)完全反应后生成水的质量为:
(2)生成的水中氧的质量为:
(3)铜的氧化物中铜的质量为:
(4)铜的氧化物中铜和氧的质量比为:
(5)计算铜的氧化物中铜、氧原子个数比为