2006-2007学年度聊城市冠县第一学期期末考试
九年级化学试卷
说明:请将第Ⅰ卷的答案涂在答题卡上,第Ⅱ卷试题答在化学答卷上,交卷时只交答题卡和 化学答卷。
相对原子质量:C―12 H一1 O―16 N一14 S―32 Na―23 Cl―35.5
第Ⅰ卷(选择题,共30分)
一、选择题(本题共15个小题,每小题2分,共30分。每小题只有一个选项正确)
1.在下列被媒体曝光的“食品事件”中,一定涉及化学变化的是( )
A.用淀粉、蔗糖、奶香精等掺和成“假奶粉”
B.用酱色、水、食盐等兑制成“假酱油”
C.用工业石蜡给瓜子“美容”
D.用硫磺燃烧后的气体熏蒸粉丝
2.下列广告用语从化学角度看,没有科学性错误的是( )
A.“霸王”牌厕所清洁剂,能清除所有污秽
B.“雪山牌”矿泉水,真正的纯水
C.吸烟有害健康
D.“大自然”牌茶叶,真正的“绿色”饮品,天然种植,不含任何元素
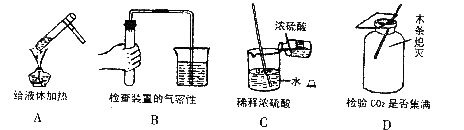
3.如图所示的几个实验操作中错误的是( )
4.用“分子的观点”解释下列现象,不正确的是( ):
A.湿衣晾干――分子不停地运动
B.干冰升华――分子间间隔变大
C.水结成冰――分子发生变化
D.轮胎充气――分子间有间隔
5.下列有关微粒的描述正确的是( )
A.原子中核内质子数和核外电子数一定相等
B.构成物质的微粒只有分子
C.钠原子失去电子变成带负电荷的钠离子
D.镁原子的质子数大于镁离子的质子数
6.要配制100g溶质的质量分数为15%的氯化钠溶液,下列操作正确的是( )
A.将15g氯化钠固体直接放在天平的托盘上称量
B.将配制好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签
C.量取85mL水时,仰视读数
D.为加快固体溶解,用温度计搅拌
7.海洛因、鸦片和大麻都是危害人类的毒品,其中大麻的化学式为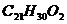 ,关于大麻的叙述正确的是(
)
,关于大麻的叙述正确的是(
)
A.大麻由21个碳元素、30个氢元素和2个氧元素组成
B.大麻中碳、氢、氧元素以单质形式存在
C.每个大麻分子由21个碳原子、30个氢原子、1个氧分子构成
D.大麻分子中碳、氢、氧元素的原子个数比为21:30:2
8.目前计入空气主要污染物的是可吸入颗粒物、一氧化碳、二氧化硫、氮的氧化物。下列情况能直接造成空气污染的是( )
A.随意丢弃塑料垃圾
B.把煤作为主要燃料
C.随意丢弃废电池
D.利用太阳能、风能等清洁能源
9.调查统计表明,火灾伤亡事故很多是由于缺乏自救常识造成的。下列自救措施中不合理的是( )
A.遇到意外的情况,可用掌握的知识进行有效处理,同时拨打电话求救
B.所处烟雾较浓时,应用湿毛巾捂住口鼻,并尽量贴近地面逃离
C.室内起火,不要急于打开所有门窗
D.在山林中遇到火灾时,向顺风方向奔跑,脱离火灾区
10.下列物质中属于纯净物的是( )
A.海水 B.自来水 C.蒸馏水 D.矿泉水
11.某同学在化学晚会上表演如下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上一种无色液体,白纸上立即出现了红色的“化学魔术”四字。该同学先后所用的无色液体可能是( )
A.紫色石蕊溶液、稀硫酸
B.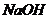 溶液、酸酞溶液
溶液、酸酞溶液
C.酚酞溶液、“雪碧”饮料
D.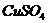 溶液、
溶液、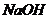 溶液
溶液
12.下列说法不正确的是( )
A.金属元素原子的最外层电子数一般少于4个
B.非金属元素的原子一般比较容易获得电子
C.单质的化合价为0
D.除氦外的稀有气体元素原子的最外层都有8个电子
13.下列说法正确的是( )
A.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
B.稀硫酸能使紫色石蕊试液变蓝
C.浓硫酸置于空气中,溶质的质量分数变大
D.露置于空气中的固体氢氧化钠,其成分不会发生变化
14.下表是各物质所含的少量杂质以及除去这些杂质所选用的试剂或操作方法,其中正确的是( )
选项
物质
杂质
除杂试剂或操作方法
A
硝酸钠溶液
硫酸钠
加入适量氯化钡溶液,再过滤
B
氯化钠溶液
氯化镁
加入适量烧碱溶液,再过滤
C
熟石灰
石灰石
高温煅烧
D
二氧化碳
一氧化碳
通过澄清石灰水
15.因废旧家用电器的电路板上含有废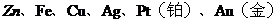 等多种贵重金属,使回收废旧电路板中的贵重金属成为一个新的行业。在回收贵重金属的过程中,经物理方法初步处理后,与足量稀盐酸充分反应,然后过滤。剩余的固体中不应有的金属是( )
等多种贵重金属,使回收废旧电路板中的贵重金属成为一个新的行业。在回收贵重金属的过程中,经物理方法初步处理后,与足量稀盐酸充分反应,然后过滤。剩余的固体中不应有的金属是( )
A.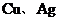 B.
B.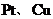 C.
C.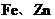 D.
D.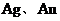
第Ⅱ卷(非选择题.共40分)
二、填空题(本题包括3个小题,共13分)
1.木糖醇是一种白色粉末状固体,它的甜度相当于蔗糖。近几年木糖醇作为新型甜味剂正在悄悄地代替蔗糖进入生活。木糖醇与蔗糖的溶解度曲线如图A所示,在口腔中细菌的作用下pH变化如图B所示。
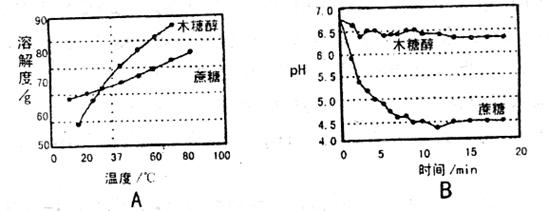
试回答:
(1)在37℃时蔗糖的溶解度_____(填“大于”、“等于”或“小于”)木糖醇的溶解度,将60℃等质量的两种物质的饱和溶液分别降温到20℃时,析出溶质质量较大的是_______。
(2)人们食用含糖量较高的物质会在口腔中细菌作用下产生酸性物质,腐蚀牙齿,形成龋齿。则食用______(填“蔗糖”或“木糖醇”)能有效的防止龋齿。
2.人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量最高的金属元素是_______。
(2)根据下图金属应用实例推断,金属具有的物理性质有_______

(3)日常使用的金属材料多数属于合金。下表列出了一些常见合金的主要成分和性能。
合金
合金的主要性能
主要成分及纯金属的性能
焊锡
熔点183℃
锡:熔点232℃;铅:熔点327℃
硬铝
强度和硬度好
铝、铜、镁等。硬度小,质软
不锈钢
抗腐蚀性好
铁、铬、镍等。纯铁抗腐蚀性能不如不锈钢
由上表推断,与组成合金的纯金属相比,合金的优点一般有(填序号)_______
①强度更低 ②硬度更高 ③熔点更高 ④抗腐蚀性更好
(4)人们每年要从金属矿物资源中提取数以亿吨计的金属。根据所学化学知识,写出一个生成金属的化学方程式:
(5)2008年奥运会主运动场“鸟巢”使用了大量的钢铁。钢铁与_______直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈。
3.新闻报道《河北秦皇岛:小雨引“燃”一车电石》称:2006年5月9日傍晚,一辆储运电石的汽车因未做好防水工作,行驶过程中天降小雨,引发车厢着火……已知:电石(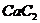 )不可燃,与水接触剧烈反应产生乙炔(
)不可燃,与水接触剧烈反应产生乙炔(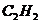 )。
)。
(1)电石与水反应属于________反应(填“吸热”成“放热)
(2)电石与水反应的化学方程式: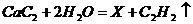 ,X的化学式为_________
,X的化学式为_________
(3)根据上述信息,请从物质组成和化学性质角度,说说你对乙炔气体的认识(各一条)。
答:组成___________
化学性质___________
(4)根据上述信息,你认为应该如何保存电石?
答:_____________
三、实验题(本题包括3小题,共16分)
4.根据化学实验操作要求,回答下列问题:
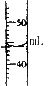
(1)酒精灯的火焰分为三层,加热时应用________部分;
(2)如图所示量取液体的体积为________
(3)实验室制取气体时,应先检查装置的__________,再加入药品;
(4)加热时,试管内液体体积最好不超过试管容积的__________
5.实验室用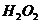 溶液和
溶液和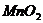 固体混合制取
固体混合制取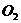 ,回答下列问题:
,回答下列问题:
(1)小红设计了如图所示的制取装置,发生反应的化学方程式是______,装置中用注射器代替长颈漏斗的优点是_______(答出一点即可)。
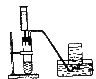
(2)同组的小刚想从反应后的混合物中分离出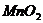 固体,其主要操作是______,此操作中必须用到的玻璃仪器是_________。
固体,其主要操作是______,此操作中必须用到的玻璃仪器是_________。
(3)小红同学将收集的氧气与空气、二氧化碳放置在一起,请问应如何区别氧气与空气、二氧化碳三瓶无色气体?(按操作→现象→结论的顺序回答)
答:__________
6.小强读了《消防知识手册》,对手册中说的“活泼金属(如镁)燃烧引发的火灾不能用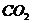 灭火”,很感兴趣。小强猜想:是不是活泼金属能与
灭火”,很感兴趣。小强猜想:是不是活泼金属能与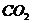 反应?他向老师要来了镁带、石灰石、盐酸和必要的器材,按下述顺序开展探究。
反应?他向老师要来了镁带、石灰石、盐酸和必要的器材,按下述顺序开展探究。
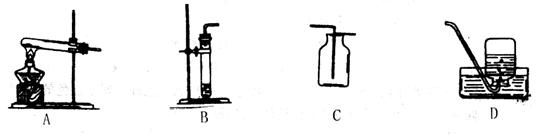
(1)制取并收集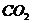 :
:
①制取CO2的化学方程式为_________。
②小强应选择图中________和________装置(填字母)制取并收集一瓶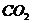 。
。
(2)开展探究:将燃烧着的镁带插入充满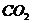 的集气瓶,镁带继续燃烧,生成一种氧化物和一种单质。该反应属于_______反应(填基本反应类型),反应的化学方程式为________。
的集气瓶,镁带继续燃烧,生成一种氧化物和一种单质。该反应属于_______反应(填基本反应类型),反应的化学方程式为________。
(3)通过实验,你对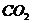 用于灭火有何新认识?
用于灭火有何新认识?
答:__________
四、计算题(本题包括2小题,共11分)
7.甜蜜素(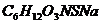 )是一种甜味添加剂。
)是一种甜味添加剂。
(1)甜蜜素的相对分子质量为__________
(2)甜蜜素中C、H、O、N、S、Na元素的质量比为_________
(3)甜蜜素中碳元素的质量分数为_________。
8.我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献。工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:
(1)该纯碱样品中碳酸钠的质量分数(计算结果精确到0.1%);
(2)反应后所得溶液中溶质的质量分数。