2005年潍坊五中中考模拟考试(三)
第一卷
相对原子质量:C-12 H-1 O-16 N-14 Cu-64 S-32 Ba-137
一、选择题(每题只有一个正确答案,每题2分,共40分)
1.下列物质属于纯净物的是( )
A.“光明”纯牛奶 B.“七星岩”岩石 C.“青岛”啤酒 D.“娃哈哈”蒸馏水
2.古诗词是古人为我们留下的宝贵精神财富。下列诗句中只涉及物理变化的是( )
A.野火烧不尽,春风吹又生
B .只要功夫深,铁杵磨成针
C .春蚕到死丝方尽,蜡炬成灰泪始干
D.爆竹声中一岁除,春风送暖入屠苏
3.下列观点,我不赞同的是
A.肥皂水可以区别硬水和软水
B.风力发电可以减少对环境的污染
C.计算机房失火只能用泡沫灭火器灭火
D.活性炭可以吸附水中的色素和异味
4.二氧化碳占空气总体积的0.03%,自然界中二氧化碳的循环如图所示,在A处不参与该循环的是:
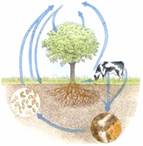
A.植物的呼吸作用;
B.含碳燃料的燃烧;
C.发展利用氢燃料;
D.人和动物的呼吸。
5.右图为我市罗星西路新近安放的分类投放垃圾箱。该垃圾箱有三个垃圾投放口分别为绿色(可回收物)、黑色(有害物)、黄色(废弃物),下表中垃圾投放正确的是……………( )
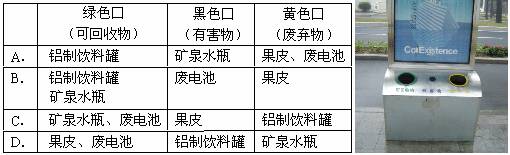
6.食品与卫生健康有着密切的联系,下列做法不会危害人体健康的是 ( )
A、为了防止水产品在运输和销售过程中变质,将水产品浸泡在甲醛溶液里
B、馒头时加入适量的纯碱
C、为了给市场提供更多的瘦肉,用“瘦肉精”(一种含激素的饲料)饲养生猪
D、提倡使用铝制餐具拒绝使用一次性木筷
7.下列物质中属于氧化物的是( )
A.KMnO4 B.NaOH C.H2SO4 D.H2O
8.下列物质的俗名与化学式不相符的是
A.纯碱(Na2CO3) B.烧碱(NaOH) C.食盐(NaCl) D.生石灰(CaCO3)
9.下列符号中的“2”与O2中的“2”含义相似的是( )
A.Cu2+ B.2O3 C.H2O D.
10.鱼味道鲜美,但剖鱼时弄破鱼胆,胆汁沾在鱼肉上,便有苦味,产生苦味的是胆汁酸,其pH约为6,且难溶于水。则在沾有胆汁的地方涂上下列物质可消除苦味的是
A.纯碱溶液 B.食醋 C.食盐水 D.自来水
11. 下列是某班四个学生分别对化学式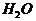 所表示意义的回答,其中错误的是( )
所表示意义的回答,其中错误的是( )
A. 表示水这种物质
B. 表示一个水分子
C. 表示一个水分子由两个氢元素和一个氧元素构成
D. 表示水由氢元素和氧元素组成
12. 导致老年人骨质疏松的主要原因是人体骨骼中缺少下列元素中的( )
A. 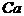 B.
B. 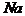 C.
C. 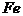 D. K
D. K
13.右图是A、B、C三种物质的溶解度曲线。下列叙述正确的是
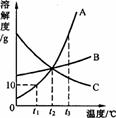
A.t3℃时,三种物质溶解度大小顺序为 A>B>C
B.tl℃时,A的饱和溶液中溶质的质量分数为10%
C.t3℃时,C的饱和溶液降温到t2℃时变成不饱和溶液
D.t1℃时,A的饱和溶液升温到t3℃时有晶体析出
14.镁带在耐高温的密闭容器(内含空气)内加热,容器内有关的量随时间变化的图像正确的是
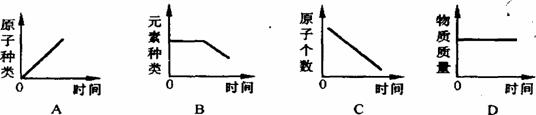
15.加碘食盐中碘元素以碘酸根(IO3-)的形式存在。已知在酸性条件下,IO3-离子能跟碘离子(I-)发生反应生成碘(I2),I2能使淀粉变蓝色。现提供下列试剂和生活中常见的物质:①碘化钾溶液(KI=K++I-) ②食醋 ③食糖 ④白酒 ⑤淀粉 ⑥纯碱,通过实验要证明加碘食盐中存在IO3-离子,必须选用的试剂和物质是( )
A.①⑤⑥ B.①②③ C.①②⑤ D.②④⑥
16.只用一种试剂可以鉴别NaOH、Ca(OH)2、稀盐酸三种溶液,这种试剂是……( )
A、硫酸铜溶液 B、硝酸银溶液 C、碳酸钠溶液 D、酚酞溶液
17.小玲同学对所学部分化学知识归纳如下,其中有错误的一组是
A
物质性质与用途
B
安全常识
N2性质稳定--填充食品袋防腐 乙醇具有可燃性--可用作燃料 CO具有还原性--可冶炼金属
假酒中毒--由甲醇引起 瓦斯爆炸--由天然气引起 假盐中毒--由黄曲霉毒素引起
C
元素与人体健康
D
日常生活经验
缺铁--易引起贫血 缺钙--易得佝偻病或骨质疏松 缺碘--易得甲状腺肿大
去除衣服上的油污--用汽油洗涤 区别硬水与软水--常用肥皂水检验 使煤燃烧更旺--把煤做成蜂窝状
18.筹建中的海峡西岸某生态农业科技园区,不仅是农业高新技术示范和推广基地,也将是一个观光休闲的生态农业园区,你认为它的下列生产思路不妥当的是……………( )
A.对大棚中植物施加适量的CO2,以促进其光合作用
B.将硝酸铵和熟石灰混合作用,在给农作物提供营养元素的同时,又能降低土壤的酸性
C.将农家肥和化肥综合使用,以提高增产效益
D. 种植、养殖、制沼气相结合,既可改善环境又可提高农畜牧业的产量
19.下列各图所示装置的气密性检查中,漏气的是 ………………………( )
20.为了测定某石灰厂的石灰中碳酸钙的质量分数,学校研究性学习小组取来了一些样品,并取稀盐酸200g,平均分成四组,进行实验,结果如下:
实验
1
2
3
4
加入样品的质量/g
5
10
15
20
生成CO2的质量/g
1.76
3.52
4.4
m
则下列推断不正确的是 ( )
A.实验2中碳酸钙恰好与稀盐酸完全反应
B.实验3中样品有剩余
C.m=4.4
D.石灰石中碳酸钙的质量分数为80%
第二卷
二、填空题(每空2分,共26分)
21.初中学习了氢、氧、碳、铁等元素的单质及化合物的知识。请回答:
(1)由H、O、C、Fe组成的常见化合物中,属于可燃性气态单质的是 ,属于无机含氧酸的是 ,属于碱的是 ,炼钢工业中常用的一种气体是 。(以上空格均填化学式)
(2)碳的几种单质物理性质不同的原因: 。
(3)用H2作燃料比CO作燃料好,主要表现在: 。
(4)一女运动员可以在60s内跑完400m,她的最大氧气吸入量为4L/min,而肌肉在工作达到极限时,每千克体重每分钟需要氧气约0.2L,如果该女运动员体重为50kg,她将缺少 L氧气。
22.(1)含氟牙膏可防龋齿,其化学式为Na2FPO3,已知F为-1价,则P的化合价为 ;含碘盐中含有碘酸钾,由K、I、O三种元素组成,其中I元素的化合价为+5价,这种化合物的化学式为 。
23.取一小块石灰石,放入试管中,加入水后滴几滴酚酞,试管里液体的颜色有无变化? (填“有”或“无”)。仍将这块石灰石取出,用滤纸吸干表面水分后,用坩埚钳夹住石灰石放在酒精灯的火焰上灼烧约2min,待冷却后小心放进试管,再加入少量水,然后再滴入几滴酚酞,这时溶液呈 色,这是因为溶液中生成了 。写出实验过程中有关反应的化学方程式 。
三、简答题
24.(5分)通过“铁”一章的学习,我们知道我国是世界上最早应用湿法冶金的国家。我们也知道,我国也是最早发明黑火药和造纸术的国家,还是最早利用天然气的国家……,根据你现在所学的化学知识,你知道化学学科有哪些“之最”?如 (1)化学变化中的最小微粒(粒子)是_________; (2)天然物质里硬度最大的物质是__________。以此为例,你还能举出3例的“化学之最”?(3) ____________________________;
(4) _______________________________________;(5) _______________________________。
25.(5分)现有以下几组试剂:①Cu 、ZnCl2溶液、AgNO3溶液,②Zn、Ag、Cu(NO3)2溶液,③Cu、Ag、 ZnSO4溶液。某兴趣小组欲用其验证Zn、Cu、Ag三种的金属活动顺序。
(1)你认为要达到实验目的,可以选用的试剂组是_______________。
(2)阿燕同学认为另外选用“Zn、Cu、AgNO3溶液”这组试剂,经过组内物质的相互反应也可验证Zn、Cu、Ag的金属活动顺序,你认为对吗__________(答对或错),
因为 。
26.(5分)小王、小李与小陈三位学生去游泳池游泳,小王对池内“蓝色水”产生好奇,引发了三人探究其中溶有什么物质的欲望。他们用一个洗净的可乐瓶盛满一瓶“蓝色水”,根据已有的经验共同讨论、设计、分工、合作进行如下实验:
分工
小王
小李
小陈
实验操作
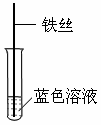
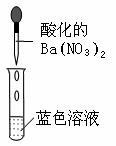
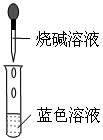
实验现象
液体内铁丝变红
产生白色沉淀
____________
实验结论
含有_________元素
白色沉淀是______
“蓝色水”中含有 溶质的化学式是________________
从这三位同学的实验过程中,你认为进行科学探究须具备__________________精神。
27.(10分)同学们到化学实验室做实验时,常常闻到刺鼻难闻的气味,这是由于化学实验室要排放成分复杂的污染物,某校化学兴趣小组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体与溶液的接触面积,使反应充分进行)。
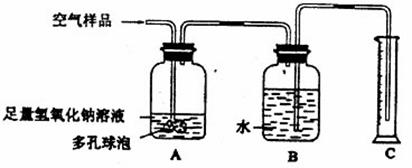
请回答下列问题:
(l)实验在没有受污染的乙实验室中进行,取出适量甲实验室的空气样品的方法是:
。
(2)将取得的空气样品按如图所示的装置进行测定,装置A的作用是 ,其中发生反应的化学方程式为: ; 。
装置B中的现象是 ;
装置C的作用是 。
(3若通入的空气样品体积为: 100 ml ,实验结束后,量筒中液体的体积为99ml(导管内液体忽略不计),说明装置 中吸收了1 ml气体,若这些气体大量排放到空气中,因产生 ,会对环境造成不利影响。
(4)请写出你在做化学实验时,减少实验对环境污染的一种做法: 。
四、计算题(9分)
28.小贝同学家买回一袋钾肥,其包装袋上的部分说明如下图所示。小贝同学取109g该钾肥,加入40g水溶解后,与足量的BaCl2溶液充分反应,并测得生成沉淀的质量为11.65g。
(1)如果钾肥的纯度(即K2SO4的质量分数)符合标准,则小贝配制的K2SO4溶液的溶质质量分数是多少?
(2)该钾肥的纯度是否符合包装袋上的说明?(K2SO4+ BaCl2ㄔBa SO4+2KCl)
附加题(本题6分,计入总分,但分数不超过试卷的满分)
29.某班级兴趣小组计划对金属与酸反应的情况进实验探究。
实验目的:探究酸的浓度对金属反应速度的影响;酸的浓度对生成氢气的量的影响。
实验原理:锌与稀硫酸反应生成氢气
实验仪器:氢气的制取和收集装置、托盘天平、量筒、秒表。
实验试剂:锌粒,5%的稀硫酸,10%的稀硫酸。
实验步骤:
实验一:称量:用托盘天平称取锌粒1.3 g,放入干燥管内;用量筒量取500 mL5%稀硫酸(足量),倒入500 mL烧杯。
如图所示连接仪器,收集氢气,记录反应时间和产生氢气的体积(如下表)。
实验二:量取500 mL10%的稀硫酸,重复上述实验,记录反应时间和生成氢气的体积(如下表)。
实验编号
锌的质量
足量稀硫酸的浓度
时间
生成氢气的体积
实验一
1.3 g
5%
169分钟
448 mL
实验二
1.3 g
10%
66分钟
448 mL
结论:
①同种金属在浓度较大的稀硫酸(或盐酸)中反应的速度____________。
②_____________________________________________________________