题目内容
12.某氧气瓶的容积V=30L,在使用过程中,氧气瓶中的压强由P1=100atm下降到P2=50atm,且温度始终保持0℃.已知在标准状况1mol气体的体积22.4L.求:使用掉的氧气分子数为多少?(阿伏加德罗常数为NA=6.0×1023mol-1,结果保留两位有效数字)分析 气体的温度不变,发生等温变化,根据玻意耳定律求出氧气瓶内的用掉的气体在标准状态的体积,再根据阿佛加德罗常数求出分子数即可.
解答 解:用气过程中,温度不变,由p1V1=p2V2,
其中p1=100 atm p2=50 atm
用掉的气体在压强是50atm时的体积为△V
△V=V2-V1=30L
设用掉的气体在标况下的体积为 V3
p2△V=p3V3
其中p3=1 atm
解得:V3=1500L
用掉的气体的分子个数:n=$\frac{{V}_{3}^{\;}}{{V}_{mol}^{\;}}{N}_{A}^{\;}$
解得:n=4.0×1025个
答:使用掉的氧气分子数为$4.0×1{0}_{\;}^{25}$个
点评 本题考查了玻意耳定律的应用,注意把变质量的问题转化为定质量的问题,还要注意把体积转化成标准状态的体积.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
5.黑洞是质量非常大的天体,由于质量很大,引起了其周围的时空弯曲,从地球上观察,我们看到漆黑一片,那么关于黑洞,你认为正确的是( )
| A. | 内部也是漆黑一片,没有任何光 | |
| B. | 内部光由于引力的作用发生弯曲,不能从黑洞中射出 | |
| C. | 内部应该是很亮的 | |
| D. | 如果有一个小的星体经过黑洞,将会被吸引进去 |
3.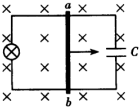 如图所示,匀强磁场的方向垂直于电路所在平面,导体棒与电路接触良好.当导体棒ab在外力F作用下从左向右做匀加速直线运动时,若不计摩擦和导线的电阻,整个过程中,灯泡L未被烧毁,电容器C未被击穿,则该过程中( )
如图所示,匀强磁场的方向垂直于电路所在平面,导体棒与电路接触良好.当导体棒ab在外力F作用下从左向右做匀加速直线运动时,若不计摩擦和导线的电阻,整个过程中,灯泡L未被烧毁,电容器C未被击穿,则该过程中( )
 如图所示,匀强磁场的方向垂直于电路所在平面,导体棒与电路接触良好.当导体棒ab在外力F作用下从左向右做匀加速直线运动时,若不计摩擦和导线的电阻,整个过程中,灯泡L未被烧毁,电容器C未被击穿,则该过程中( )
如图所示,匀强磁场的方向垂直于电路所在平面,导体棒与电路接触良好.当导体棒ab在外力F作用下从左向右做匀加速直线运动时,若不计摩擦和导线的电阻,整个过程中,灯泡L未被烧毁,电容器C未被击穿,则该过程中( )| A. | 感应电动势将变大 | B. | 电容器C的上极板带负电 | ||
| C. | 电容器两极板间的电场强度将减小 | D. | 灯泡的亮度变大 |
20.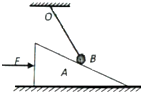 如图所示,一根细绳的上端系在O点,下端系一个重球B,重球B放在粗糙的倾角为θ的斜面体A上,已知小球B与斜面间的动摩擦因数μ=$\frac{1}{tanθ°}$,现用水平推力F向右推斜面体,使之在光滑水平面上缓慢向右运动一段距离(细绳尚未到达平行于斜面的位置),在此过程中,下列说法正确的是 ( )
如图所示,一根细绳的上端系在O点,下端系一个重球B,重球B放在粗糙的倾角为θ的斜面体A上,已知小球B与斜面间的动摩擦因数μ=$\frac{1}{tanθ°}$,现用水平推力F向右推斜面体,使之在光滑水平面上缓慢向右运动一段距离(细绳尚未到达平行于斜面的位置),在此过程中,下列说法正确的是 ( )
 如图所示,一根细绳的上端系在O点,下端系一个重球B,重球B放在粗糙的倾角为θ的斜面体A上,已知小球B与斜面间的动摩擦因数μ=$\frac{1}{tanθ°}$,现用水平推力F向右推斜面体,使之在光滑水平面上缓慢向右运动一段距离(细绳尚未到达平行于斜面的位置),在此过程中,下列说法正确的是 ( )
如图所示,一根细绳的上端系在O点,下端系一个重球B,重球B放在粗糙的倾角为θ的斜面体A上,已知小球B与斜面间的动摩擦因数μ=$\frac{1}{tanθ°}$,现用水平推力F向右推斜面体,使之在光滑水平面上缓慢向右运动一段距离(细绳尚未到达平行于斜面的位置),在此过程中,下列说法正确的是 ( )| A. | 水平推力F为恒力 | B. | 斜面体A对重球B的作用力水平向右 | ||
| C. | 细绳对重球B的拉力不断增大 | D. | 细绳对重球B的拉力先减小后增大 |
17.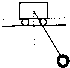 如图所示,一辆小车静止在光滑的水平导轨上,一个小球用细绳悬挂在车上,由图中位置无初速释放,则小球在下摆过程中,下列说法错误的是( )
如图所示,一辆小车静止在光滑的水平导轨上,一个小球用细绳悬挂在车上,由图中位置无初速释放,则小球在下摆过程中,下列说法错误的是( )
 如图所示,一辆小车静止在光滑的水平导轨上,一个小球用细绳悬挂在车上,由图中位置无初速释放,则小球在下摆过程中,下列说法错误的是( )
如图所示,一辆小车静止在光滑的水平导轨上,一个小球用细绳悬挂在车上,由图中位置无初速释放,则小球在下摆过程中,下列说法错误的是( )| A. | 绳对小球的拉力做负功 | B. | 小球和小车组成的系统机械能守恒 | ||
| C. | 小球机械能不守恒 | D. | 小球和小车组成的系统动量守恒 |
1.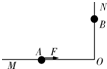 如图所示,MON是固定的光滑绝缘直角杆,MO沿水平方向,NO沿竖直方向,A、B为两个套在此杆上的带有同种电荷的小球.用一指向竖直杆的水平力F作用在A球上,使两球均处于静止状态.现将A球向竖直杆方向缓慢拉动一小段距离后,A、B两小球可以重新平衡.则后一种平衡状态与前一种平衡状态相比较,下列说法正确的是( )
如图所示,MON是固定的光滑绝缘直角杆,MO沿水平方向,NO沿竖直方向,A、B为两个套在此杆上的带有同种电荷的小球.用一指向竖直杆的水平力F作用在A球上,使两球均处于静止状态.现将A球向竖直杆方向缓慢拉动一小段距离后,A、B两小球可以重新平衡.则后一种平衡状态与前一种平衡状态相比较,下列说法正确的是( )
 如图所示,MON是固定的光滑绝缘直角杆,MO沿水平方向,NO沿竖直方向,A、B为两个套在此杆上的带有同种电荷的小球.用一指向竖直杆的水平力F作用在A球上,使两球均处于静止状态.现将A球向竖直杆方向缓慢拉动一小段距离后,A、B两小球可以重新平衡.则后一种平衡状态与前一种平衡状态相比较,下列说法正确的是( )
如图所示,MON是固定的光滑绝缘直角杆,MO沿水平方向,NO沿竖直方向,A、B为两个套在此杆上的带有同种电荷的小球.用一指向竖直杆的水平力F作用在A球上,使两球均处于静止状态.现将A球向竖直杆方向缓慢拉动一小段距离后,A、B两小球可以重新平衡.则后一种平衡状态与前一种平衡状态相比较,下列说法正确的是( )| A. | A、B两小球间的库仑力变大,B球对NO杆的压力变大 | |
| B. | A、B两小球间的库仑力变小,B球对NO杆的压力变小 | |
| C. | A、B两小球间的库仑力变小,A球对MO杆的压力变小 | |
| D. | A、B两小球间的库仑力变大,A球对MO杆的压力不变 |
1.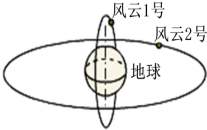 我国在轨运行的气象卫星有两类,一类是极地轨道卫星-风云1号,绕地球做匀速圆周运动的周期为12h,另一类是地球同步轨道卫星-风云2号,运行周期为24h.下列说法正确的是( )
我国在轨运行的气象卫星有两类,一类是极地轨道卫星-风云1号,绕地球做匀速圆周运动的周期为12h,另一类是地球同步轨道卫星-风云2号,运行周期为24h.下列说法正确的是( )
 我国在轨运行的气象卫星有两类,一类是极地轨道卫星-风云1号,绕地球做匀速圆周运动的周期为12h,另一类是地球同步轨道卫星-风云2号,运行周期为24h.下列说法正确的是( )
我国在轨运行的气象卫星有两类,一类是极地轨道卫星-风云1号,绕地球做匀速圆周运动的周期为12h,另一类是地球同步轨道卫星-风云2号,运行周期为24h.下列说法正确的是( )| A. | 风云1号的线速度大于风云2号的线速度 | |
| B. | 风云1号的向心加速度小于风云2号的向心加速度 | |
| C. | 风云1号的发射速度大于风云2号的发射速度 | |
| D. | 风云1号、风云2号相对地面均静止 |