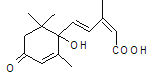
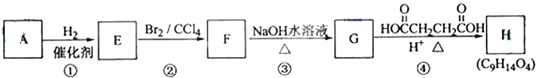
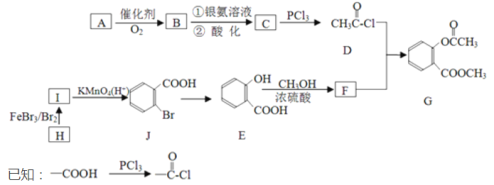
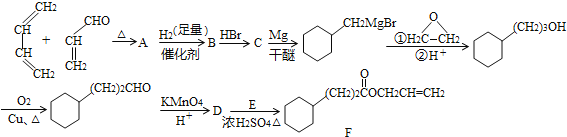
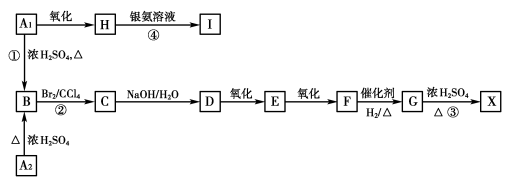
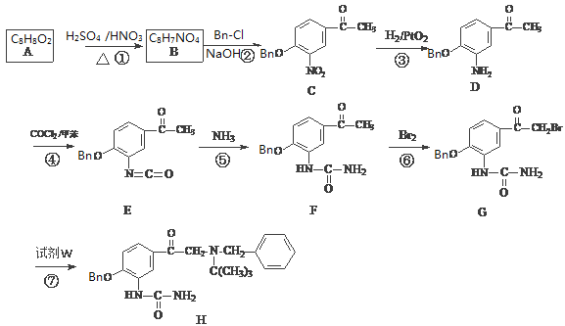
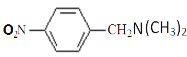
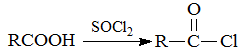题目内容
【题目】实验室常用如图所示装置制取少量乙酸乙酯。请回答下列问题:
(1)试管a中需加入浓硫酸、乙酸各2 mL,乙醇3 mL,应该先加入________,再入________,最后加入________。

(2)试管a中发生反应的化学方程式是________________,反应类型是________,通常加入几片碎瓷片,其作用是_______________________________________________________。
(3)试管b中加入饱和Na2CO3溶液,其作用是______________________________________。
(4)反应结束后,振荡试管b,静置。观察到的现象_________________________________。
【答案】(1)乙醇,浓硫酸,乙酸;(2)C2H5OH+CH3COOH ![]() CH3COOC2H5+H2O,取代反应,防暴沸;(3)反应掉挥发出来的乙酸;溶解挥发出来的乙醇;减小乙酸乙酯的溶解度,使溶液分层,便于得到乙酸乙酯;(4)试管b中的液体分层,上层是透明的油状液体。
CH3COOC2H5+H2O,取代反应,防暴沸;(3)反应掉挥发出来的乙酸;溶解挥发出来的乙醇;减小乙酸乙酯的溶解度,使溶液分层,便于得到乙酸乙酯;(4)试管b中的液体分层,上层是透明的油状液体。
【解析】
试题分析:(1)浓硫酸的浓度大于乙醇,密度大的加入到密度小的液体中,防止受热不均,造成液体飞溅,乙醇比较廉价,因此所加顺序是乙醇、浓硫酸、乙酸;(2)试管中发生酯化反应,依据酸去羟基醇去氢,其反应方程式为:C2H5OH+CH3COOH ![]() CH3COOC2H5+H2O,取代反应或酯化反应,因为都是液体参加反应,需要加热,为防止暴沸,需要加入碎瓷片或沸石;(3)挥发出的乙酸乙酯中含有乙酸和乙醇杂质,饱和碳酸钠的作用是①吸收乙醇②除去乙酸③降低乙酸乙酯在溶液中溶解度,使之析出;(4)乙酸乙酯为液体,且密度小于水,不溶于水,出现分层现象。
CH3COOC2H5+H2O,取代反应或酯化反应,因为都是液体参加反应,需要加热,为防止暴沸,需要加入碎瓷片或沸石;(3)挥发出的乙酸乙酯中含有乙酸和乙醇杂质,饱和碳酸钠的作用是①吸收乙醇②除去乙酸③降低乙酸乙酯在溶液中溶解度,使之析出;(4)乙酸乙酯为液体,且密度小于水,不溶于水,出现分层现象。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案