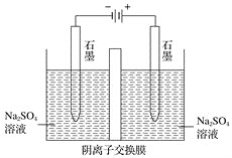
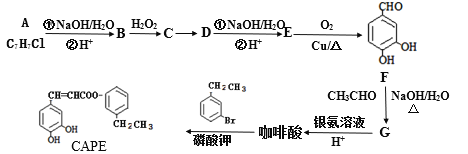
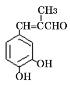
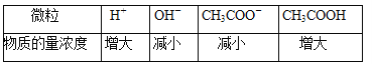
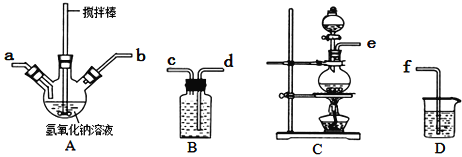
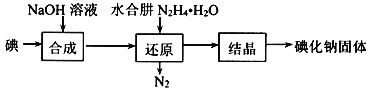
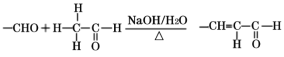0 202646 202654 202660 202664 202670 202672 202676 202682 202684 202690 202696 202700 202702 202706 202712 202714 202720 202724 202726 202730 202732 202736 202738 202740 202741 202742 202744 202745 202746 202748 202750 202754 202756 202760 202762 202766 202772 202774 202780 202784 202786 202790 202796 202802 202804 202810 202814 202816 202822 202826 202832 202840 203614