【题目】下列说法正确的是![]()
A.![]() 有机物
有机物![]() 的分子结构中含有的
的分子结构中含有的![]() 键数目一定为
键数目一定为![]()
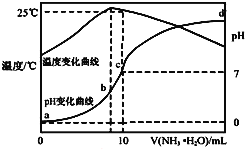
B.一定温度下,氯化铵水解离子方程式:![]() ,若用
,若用![]() 表示的离子积,
表示的离子积,![]() 表示氨水电离常数,则氯化铵水解平衡常数
表示氨水电离常数,则氯化铵水解平衡常数![]()
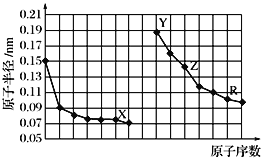
C.已知反应:![]() :
:![]() :
:![]() ;则在酸性溶液中氧化性:
;则在酸性溶液中氧化性:![]()
D.已知
共价键 |
|
|
|
|
键能 | 360 | 436 | 431 | 176 |
则反应![]() 的焓变为:
的焓变为:![]()
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺如下:

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有___________、__________。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:___________。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | —— | —— | —— |
沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有___________;但溶液的pH不能超过8,其理由是_____________________。
(4)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是_______。