【题目】硒鼓回收料含硒约![]() ,其余为约
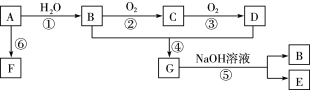
,其余为约![]() 的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示
的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示![]() 已知煅烧过程中,回收料中的硒、碲被氧化成
已知煅烧过程中,回收料中的硒、碲被氧化成![]() 和
和![]() :
:
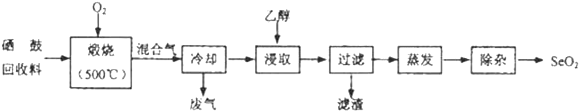
部分物质的物理性质如表:
物质 | 熔点 | 沸点 | 溶解度 |
|
|
| 易溶于水和乙醇 |
|
|
| 微溶于水,不溶于乙醇 |
回答下列问题:
(1)![]() 与S是同族元素,比S多1个电子层,Se在元素周期表的位置为______;
与S是同族元素,比S多1个电子层,Se在元素周期表的位置为______;![]() 的热稳定性比
的热稳定性比![]() 的热稳定性______
的热稳定性______![]() 填“强”或“弱”
填“强”或“弱”![]() .
.
(2)乙醇浸取后过滤所得滤渣的主要成分是______![]() 蒸发除去溶剂后,所得固体中仍含有少量
蒸发除去溶剂后,所得固体中仍含有少量![]() 杂质,除杂时适宜采用的方法是______.
杂质,除杂时适宜采用的方法是______.
(3)![]() 易溶于水得到
易溶于水得到![]() 溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式______.
溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式______.
(4)已知![]() 的电离常数
的电离常数![]() 、
、![]() ,回答下列问题:
,回答下列问题:
![]() 溶液呈______性,原因是
溶液呈______性,原因是![]() 用离子方程式表示
用离子方程式表示![]() ______;
______;
![]() 在
在![]() 溶液中,下列关系式正确的是______:
溶液中,下列关系式正确的是______:
A.![]()
B.![]()
C.![]()
D.![]()