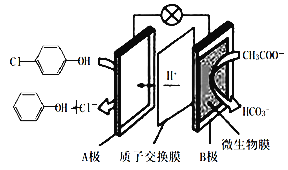
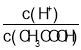【题目】研究氮族元素有关物质的结构、性质和转化有重要意义。
⑴已知P4、P4O6的结构及所含化学键键能如下:
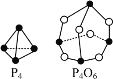
化学键 | P-P | P-O | O=O |
键能(kJ·mol-1) | a | b | c |
则P4燃烧的热化学反应方程式:P4(s)+3O2(g)=P4O6(s) ΔH=_______kJ·mol-1。
⑵亚磷酸(H3PO3) 是一种精细化工产品。已知25℃时,亚磷酸(H3PO3)的Ka1=5×10-2,Ka2=2.5×10-7。0.1 mol·L-1 NaH2PO3溶液中H3PO3、H2PO![]() 、HPO
、HPO![]() 的浓度由大到小的顺序是_______。
的浓度由大到小的顺序是_______。
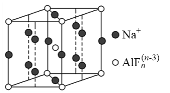
⑶雌黄(As2S3)和雄黄(As4S4)早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。一定条件下,雌黄和雄黄的转化关系如图1所示。
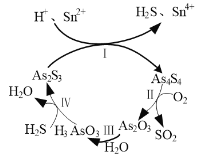
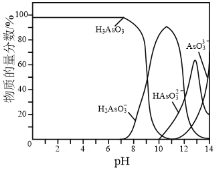
图1 图2
①反应Ⅰ的离子方程式为______。
②反应Ⅱ中,若1 mol As4S4参加反应,转移电子的物质的量为______。
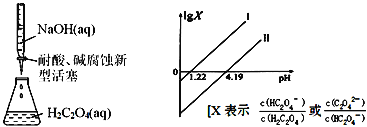
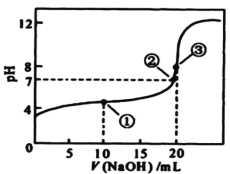
⑷常温下,用NaOH溶液滴定H3AsO3溶液,含As微粒的物质的量分数随pH的变化如图2所示。
①将NaOH溶液滴加到滴有酚酞的H3AsO3溶液中,当溶液由无色变为红色时主要反应的离子方程式为______。
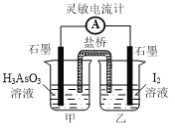
②一定条件下H3AsO3可发生如下反应: H3AsO3+I2+H2O![]() H3AsO4+2H++2I-利用该反应可设计如图所示的原电池。负极的电极反应式为_______。当反应达到平衡后,向甲中加
H3AsO4+2H++2I-利用该反应可设计如图所示的原电池。负极的电极反应式为_______。当反应达到平衡后,向甲中加
入NaOH,盐桥中阴离子_______(填“向甲池”、 “向乙池”或“不”)移动。