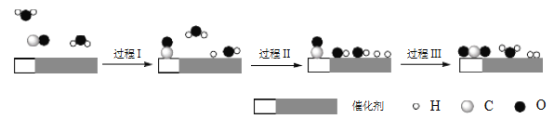
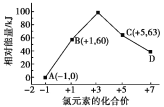
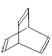
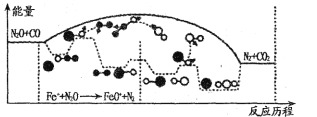
0 199406 199414 199420 199424 199430 199432 199436 199442 199444 199450 199456 199460 199462 199466 199472 199474 199480 199484 199486 199490 199492 199496 199498 199500 199501 199502 199504 199505 199506 199508 199510 199514 199516 199520 199522 199526 199532 199534 199540 199544 199546 199550 199556 199562 199564 199570 199574 199576 199582 199586 199592 199600 203614