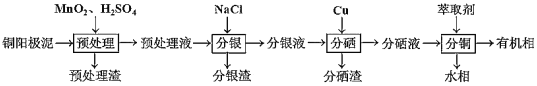
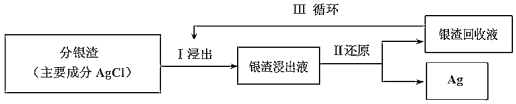
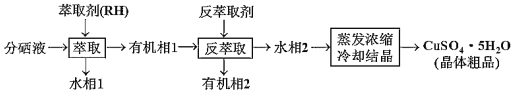
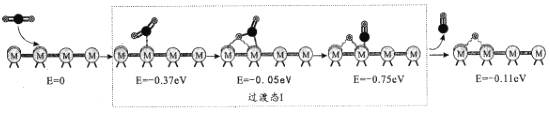
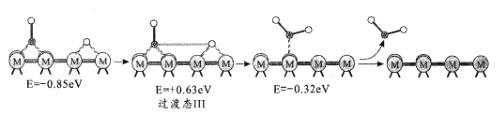
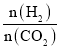【题目】绪(Ge)是半导体元素,应用广泛,回答下列问题:
(1)下列为Ge价电子层电子排布图表示的状态中,能量最低和最高的分别为____、_____(填选项)。
A.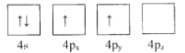 B.
B.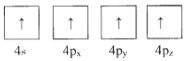
C.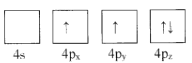 D.
D.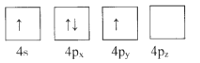
(2)GeH4的空间构型为____;比较与同锗族的氢化物的沸点如表所示,分析其变化规律及原因____。
CH4 | SiH4 | GeH4 | |
沸点/℃ | -161.5 | -119 | -88.1 |
(3)有机锗化合物A有一定的医疗保健作用,其结构简式为CF3N=GeH2,则Ge的杂化形式为____,碳原子与其它原子结合的键的种类为_____。
(4)Li2GeF6可以作为锂电池的电解质,则Li、Ge、F电负性由大到小的顺序为_____。
(5)Ge晶胞如下,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() ),D为(
),D为(![]() ,
,![]() ,
,![]() )。则C原子的坐标参数为_____。
)。则C原子的坐标参数为_____。
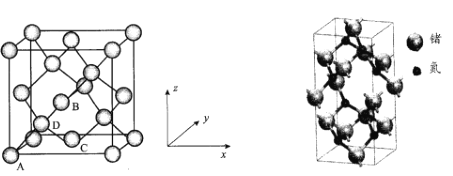
(6)氮化锗具有耐腐蚀、硬度高等优点,晶体中锗原子与氮原子之间存在明显的s-p杂化现象,氮化锗晶体属于____晶体。一种氮化锗晶胞的球棍模型如图,晶体中n(Ge)/n(N)=____,若晶胞底面正方形的边长为anm,阿伏加德罗常数值为NA,晶体的密度为ρg/cm3,则长方体的高为____nm(列出计算式)。