【题目】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
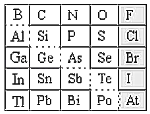
(1)元素Ga在元素周期表中的位置为:__________(写明周期和族)。
(2)Sn的最高正价为______,Cl的最高价氧化物对应水化物的化学式为_____,As的气态氢化物为_____。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_____(填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_____H2SeO4(填“>”、“<”或“=”)。
③氢化物的还原性:H2O_____H2S(填“>”、“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找_____(填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(5)①Se2Cl2常用作分析试剂,其电子式为_________。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。 下列说法正确的是_____(填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(6)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
实验步骤 | 实验现象与结论 |
在试管中加入_____,再加入_____,将生成气体通过_____洗气后,通入_____; | 现象:__________; 结论:非金属性C>Si |