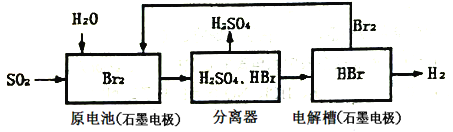
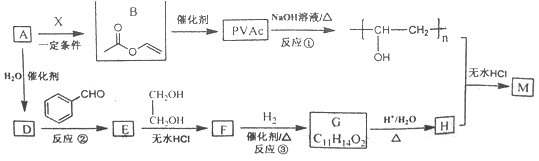
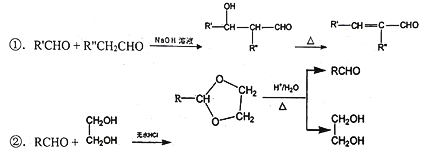
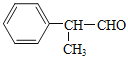
0 194247 194255 194261 194265 194271 194273 194277 194283 194285 194291 194297 194301 194303 194307 194313 194315 194321 194325 194327 194331 194333 194337 194339 194341 194342 194343 194345 194346 194347 194349 194351 194355 194357 194361 194363 194367 194373 194375 194381 194385 194387 194391 194397 194403 194405 194411 194415 194417 194423 194427 194433 194441 203614