0 175306 175314 175320 175324 175330 175332 175336 175342 175344 175350 175356 175360 175362 175366 175372 175374 175380 175384 175386 175390 175392 175396 175398 175400 175401 175402 175404 175405 175406 175408 175410 175414 175416 175420 175422 175426 175432 175434 175440 175444 175446 175450 175456 175462 175464 175470 175474 175476 175482 175486 175492 175500 203614
 2NO(g)+O2(g)。在三种不同的条件下进行实验,NO2 的浓度随时间的变化如图所示。请回答下列问题:
2NO(g)+O2(g)。在三种不同的条件下进行实验,NO2 的浓度随时间的变化如图所示。请回答下列问题:

 、
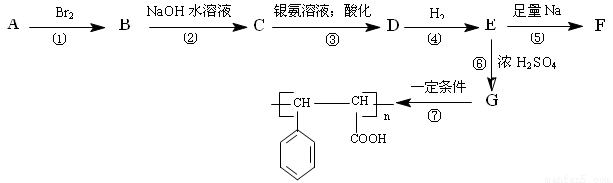
、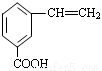 请写出其他两种 ________、________。
请写出其他两种 ________、________。