题目内容
NO2 压缩成 N2O4 可作火箭燃料中的氧化剂,也可 制备硝化试剂 N2O5 等。
(1)火箭燃料燃烧反应如下:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l),若 1.00 g N2H4(l)与足量 N2O4(l)完全反应生成 N2(g)和 H2O(l),放出 19.14 kJ 的热量。则该反应的△H=___________kJ/mol。
(2)在 2 L 密闭容器内,投入一定量 NO2,发生下列反应: 2NO2(g)  2NO(g)+O2(g)。在三种不同的条件下进行实验,NO2 的浓度随时间的变化如图所示。请回答下列问题:
2NO(g)+O2(g)。在三种不同的条件下进行实验,NO2 的浓度随时间的变化如图所示。请回答下列问题:

①不能说明该反应已达到平衡状态的是___________________(填字母)。
a.v 正(NO2)=2v 逆(O2)
b.c(NO2)= c(NO)
c.气体总压不变
d.NO 的体积分数保持不变
②下列说法正确的是___________________(填字母)。
a.三个实验开始投入的 NO2 的物质的量均为 1.0 mol
b.实验Ⅱ和实验Ⅰ相比,可能隐含的条件是:实验Ⅱ使用了效率更高的催化剂
c.该反应是放热反应
d.实验Ⅰ条件下反应的平衡常数大于实验Ⅲ条件下反应的平衡常数
e.800℃时,该反应的平衡常数为 0.25
f.该反应的△S>0,故该反应一定是自发反应
③实验Ⅱ从反应开始到刚达到平衡时,v(O2)=_________ mol/(L·min)
若再向该 2 L 密闭容器中通入 1 mol NO2、1 mol NO、0.5 mol O2,则平衡将 移动(填“向右”、“向左”或“不”)。
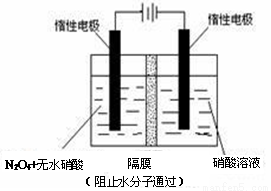
(3)利用 NO2 或 N2O4 可制备 N2O5,原理如上图所示。N2O5 在电解池的 ________(填“阴极”或“阳极”)区生成,其电极反应式为___________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案

 g C.
g C.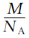 g D.
g D.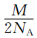 g
g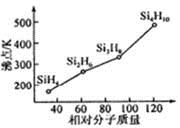



 SO2、C2H4、O2等气体
SO2、C2H4、O2等气体 CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( ) 反应方向移动
反应方向移动