15.下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 100ml 0.5mol/L MgCl2溶液 | B. | 200ml 0.25mol/L HCl溶液 | ||
| C. | 50ml 1mol/L NaCl溶液 | D. | 200ml 0.25mol/L CaCl2溶液 |
14.某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转.一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是( )
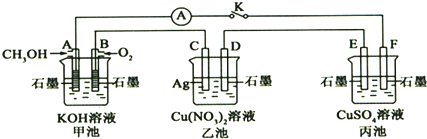

| A. | Cu | B. | CuO | C. | Cu(OH)2 | D. | Cu2(OH)2CO3 |
13.下列叙述正确的是( )
| A. | 氯化铵、次氯酸钠、醋酸铵、硫酸钡都是强电解质 | |
| B. | 电解、电泳、电离、电化学腐蚀均需在通电条件下才能进行 | |
| C. | 红宝石、水晶、钻石的主要成分都是二氧化硅 | |
| D. | 福尔马林、水玻璃、氨水、胆矾均为混合物 |
12.下列事实不能用勒沙特列原理解释的是( )
①铁在潮湿的空气中容易生锈;
②实验室可用排饱和食盐水的方法收集氯气;
③常温下,将1mL pH=3的醋酸溶液加水稀释至100mL,测得其pH<5;
④钠与氯化钾共融制备钾Na(1)+KCl(1)K(g)+NaCl(1);
⑤二氧化氮与四氧化二氮的平衡体系,加压后颜色加深.
①铁在潮湿的空气中容易生锈;
②实验室可用排饱和食盐水的方法收集氯气;
③常温下,将1mL pH=3的醋酸溶液加水稀释至100mL,测得其pH<5;
④钠与氯化钾共融制备钾Na(1)+KCl(1)K(g)+NaCl(1);
⑤二氧化氮与四氧化二氮的平衡体系,加压后颜色加深.
| A. | 只有①②③ | B. | 只有①⑤ | C. | 只有③④⑤ | D. | 只有②⑤ |
10.下列叙述正确的是( )
| A. | 使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高 | |
| B. | 78 gNa2O2溶于1 L水配成溶液,可得到1 mol•L-1 NaOH溶液 | |
| C. | 标准状况下22.4LH2O所含分子数为NA | |
| D. | 100mL0.2mol•L-1的FeCl3溶液中,含Fe3+数为0.02NA |
9.下列是生活中常见的几种药物,
阿司匹林: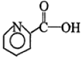 芬必得:
芬必得: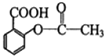
扑热息痛: 维生素B5:
维生素B5: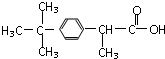
有关这些物质的说法正确的是( )
阿司匹林:
 芬必得:
芬必得:
扑热息痛:
 维生素B5:
维生素B5:
有关这些物质的说法正确的是( )
| A. | 都含有苯环 | B. | 碳原子都共平面 | ||
| C. | 都能与Na2CO3反应 | D. | 都能水解 |
6.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
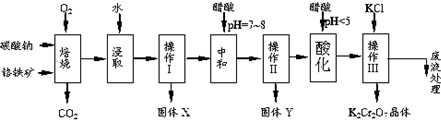
已知:①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑;③Cr2O72-+H2O═2CrO42-+2H+.根据题意回答下列问题:
(1)固体X中主要含有Fe2O3、MgO(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸(填写仪器或试剂名称).
(2)酸化步骤用醋酸调节溶液pH<5,其目的是使CrO42-转化为Cr2O72-.
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)如表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.该反应在溶液中能发生的理由是K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量是称取n g样品,加入过量NaOH溶液(填写试剂)、溶解、过滤、再通入过量二氧化碳(填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26m}{17n}$(用含m、n的代数式表示).
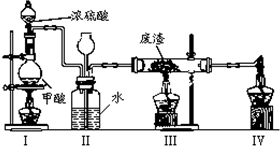
(6)六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如图:CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是III、I、IV.
0 173683 173691 173697 173701 173707 173709 173713 173719 173721 173727 173733 173737 173739 173743 173749 173751 173757 173761 173763 173767 173769 173773 173775 173777 173778 173779 173781 173782 173783 173785 173787 173791 173793 173797 173799 173803 173809 173811 173817 173821 173823 173827 173833 173839 173841 173847 173851 173853 173859 173863 173869 173877 203614

已知:①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑;③Cr2O72-+H2O═2CrO42-+2H+.根据题意回答下列问题:
(1)固体X中主要含有Fe2O3、MgO(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸(填写仪器或试剂名称).
(2)酸化步骤用醋酸调节溶液pH<5,其目的是使CrO42-转化为Cr2O72-.
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)如表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.该反应在溶液中能发生的理由是K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
(6)六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如图:CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是III、I、IV.

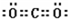 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.