题目内容
6.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图: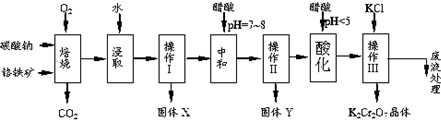
已知:①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑;③Cr2O72-+H2O═2CrO42-+2H+.根据题意回答下列问题:
(1)固体X中主要含有Fe2O3、MgO(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸(填写仪器或试剂名称).
(2)酸化步骤用醋酸调节溶液pH<5,其目的是使CrO42-转化为Cr2O72-.
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)如表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.该反应在溶液中能发生的理由是K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
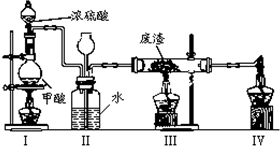
(6)六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如图:CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是III、I、IV.
分析 铬铁矿通过焙烧,生成Na2CrO4、Fe2O3、MgO和NaAlO2的混合体系,然后加水溶解得固体Fe2O3、MgO和溶液Na2CrO4、NaAlO2,再调节溶液的PH,使偏铝酸盐完全沉淀,继续调节溶液的PH使CrO42-转化为Cr2O72-,最后向所得溶液中加入氯化钾,生成溶解度极小的K2Cr2O7,
(1)依据流程图和题干反应分析判断固体X的成分;通常PH试纸只能测定溶液PH的整数,测定PH是小数的需要用精确试纸或pH计;
(2)结合流程图和反应过程中得到物质分析,酸化步骤用醋酸调节溶液pH<5为了转化CrO42-离子为Cr2O72-;
(3)溶液中得到溶质晶体的方法是蒸发浓缩,冷却结晶,过滤洗涤步骤分析回答;
(4)依据物质溶解度比较分析,反应向溶解度晓得方向进行;
(5)利用氢氧化铝是两性氢氧化物和强碱反应溶解,少量镁、铁的难溶化合物不溶解;分离提取溶液中的偏铝酸钠可以根据实验室制取氢氧化铝沉淀的方法进行,通入二氧化碳得到氢氧化铝沉淀;灼烧后得到氧化铝,依据元素守恒计算得到;
(6)用CO还原CrO3制取Cr,实验结束时,为防止金属被氧化,在停止III加热时,继续通入CO,一氧化碳有毒,所以尾气处理时酒精灯应最后熄灭,据此解答;
解答 解:(1)铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,加入氧气和碳酸钠,发生反应为:
①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑;
③Cr2CO72-+H2O?2CrO42-+2H+
操作Ⅰ是过滤得到固体X为Fe2O3、MgO;要检测酸化操作中溶液的pH是否等于4.5,普通pH试纸只能测定溶液pH到整数,是近似测定,准确测定需要用pH计或精确pH试纸,
故答案为:Fe2O3、MgO;pH计或精密pH试纸;
(2)酸化步骤用醋酸调节溶液pH<5,依据流程图中物质的转化和制备目的可知,结合反应平衡Cr2O72-+H2O?2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72-,
故答案为:使CrO42-转化为Cr2O72-;
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩,冷却结晶、过滤、洗涤、干燥得到晶体,
故答案为:冷却结晶;洗涤;
(4)依据图表物质的溶解度分析对比,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl;说明K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小),
故答案为:K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小);
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是先利用氢氧化铝的两性,用氢氧化钠溶液溶解氢氧化铝过滤得到滤液中通入二氧化碳生成氢氧化铝沉淀,灼烧干燥得到氧化铝干燥固体m g,依据铝元素守恒计算,样品中氢氧化铝的质量分数=$\frac{\frac{mg}{156g/mol}×2×78g/mol}{ng}$=$\frac{26m}{17n}$,
故答案为:NaOH溶液;通入过量二氧化碳;$\frac{26m}{17n}$;
(6)Ⅰ为制备CO装置,用CO还原CrO3制取Cr,实验结束时,为防止金属被氧化,在停止III加热时,应继续加热I,一氧化碳有毒,所以尾气处理时酒精灯应最后熄灭,所以结束时正确的熄灯顺序为:III、I、IV,
故答案为:III、I、IV.
点评 本题考查了物质制备流程和方案的分析判断,物质性质的应用,题干信息的分析理解,操作步骤的注意问题和基本操作方法是解题关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案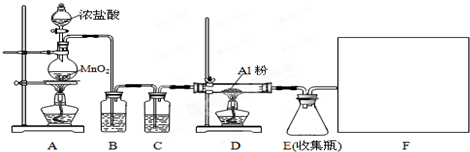
(1)A装置中发生反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)装置B的作用是除去Cl2中混有的HCl气体.
(3)请给标记为F的实线方框选择合适的装置III.
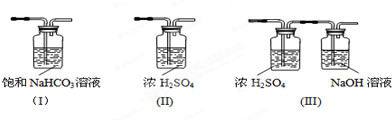
(4)AlCl3遇潮湿空气即产生大量白雾的原因是AlCl3遇水水解,Al3++3H2O?Al(OH)3+3H+,产生的氯化氢气体在空气中形成酸雾(结合化学方程式说明).
(5)有同学认为装置E中有不足之处,存在安全隐患.若你同意他的观点,请指出其不足之处连接D、E间导管太细,生成的无水AlCl3易凝固导气管堵塞.
(6)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,该小组同学提出酸碱中和滴定法测定方案.方案如下:首先准确量取残余清液稀释一定的倍数后作为试样,平行做了4次滴定.实验中所用NaOH溶液浓度为0.2000mol•L-1,以下是实验记录与数据处理(不考虑NaOH与残液中其他成分的反应).
| 滴定次数 实验数据ml | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(初读数) | 0.00 | 0.50 | 0.70 | 1.00 |
| V(NaOH)终读数) | 22.60 | 22.55 | 22.65 | 23.00 |
②在本实验的滴定过程中,下列操作会使实验结果偏小的是df(填写序号).
a.开始滴定时滴定管尖嘴处留有气泡,滴定结束气泡消失
b.未用标准NaOH溶液润洗滴定管
c.锥形瓶中加入待测盐酸后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前锥形瓶用待测盐酸润洗
f.观察读数时,滴定前仰视,滴定后俯视
海水粗盐试剂Ⅰ苦卤水(含K+、Mg2+、Br?等)MgMg(OH)2沉淀蒸发结晶┉┉
| A. | 挥发 | B. | 电解 | C. | 萃取 | D. | 蒸馏 |
①向饱和Na2CO3溶液中通入过量的CO2
②向Na2SiO3溶液中逐滴加入过量稀硫酸
③向Ba(NO3)2溶液中通入过量的SO2
④向石灰水中通入过量的CO2气体
⑤向AlCl3溶液中逐滴滴加NaOH溶液至过量.
| A. | ①②③④ | B. | ①②⑤ | C. | ①②③⑤ | D. | ①②③ |
| A. | 1molFe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| B. | 50ml18.4mol•L-1浓H2SO4与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| C. | 将含3NA个离子的Na2O2固体溶于水配成1L溶液,所得溶液中Na+的浓度为2mol•L-1 | |
| D. | 标况状态下,22.4L氨水含有NA个NH3分子 |