16.下列各组物质中,互为同素异形体的是( )
| A. | 16O和18O | B. | 白磷和红磷 | C. | 氨气和液氨 | D. | H2和D2 |
12.对于常温下pH=2的盐酸,下列叙述正确的是( )
| A. | c(H+)=c(Cl-)+c(OH-) | |
| B. | 适量升高温度,溶液的pH和Kw都变小 | |
| C. | 与等体积pH=12的氨水混合后所得溶液的pH<7 | |
| D. | 与等体积0.03mol/LNaOH溶液混合前后,H2O电离出的c(H+)没发生变化 |
11.下列根据实验事实所得结论或解释正确的是( )
| 实验事实 | 结论或解释 | |
| A | SO2的水溶液导电 | SO2是电解质 |
| B | AlCl3溶液导电 | AlCl3是离子化合物 |
| C | H2SO4溶液导电性比CH3COOH溶液强 | H2SO4是强电解质 |
| D | 0.1mol/LCH3COOH溶液的pH>1 | CH3COOH?H++CH3COO- |
| A. | A | B. | B | C. | C | D. | D |
10. 在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0
在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0
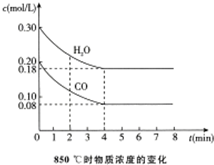
(1)850℃时,通入一定量的CO和H2O,CO和H2O浓度变化如图.
①0~4min的平均反应速率v(CO)=0.03mol/(L•min).
②850℃时,该反应的平衡常数K=1.
t1℃时物质浓度(mol/L)的变化
(2)t1℃时,在相同容器中发生上述反应,容器内各物质的浓度数据如上表.
①上述两个温度下进行的反应,先达到化学平衡状态的温度是t1℃.
②c1>(填“>”“<”或“=”)0.08mol/L.
③反应在4min~5min之间时,若平衡逆向移动,可能的原因是d,表中5min~6min之间数值发生变化,可能的原因是a.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
 在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0
在容积为10L的容器中,850℃和t1℃(高于850℃)时分别发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0(1)850℃时,通入一定量的CO和H2O,CO和H2O浓度变化如图.
①0~4min的平均反应速率v(CO)=0.03mol/(L•min).
②850℃时,该反应的平衡常数K=1.
t1℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①上述两个温度下进行的反应,先达到化学平衡状态的温度是t1℃.
②c1>(填“>”“<”或“=”)0.08mol/L.
③反应在4min~5min之间时,若平衡逆向移动,可能的原因是d,表中5min~6min之间数值发生变化,可能的原因是a.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
9.在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1)
用符号“>”“<”“=”或数字填空:
(1)α1+α2=1.
(2)a+b=92.4.
(3)2c1<c3
(4)2p2>p3
(5)α1+α3=<1.
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2,3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
(1)α1+α2=1.
(2)a+b=92.4.
(3)2c1<c3
(4)2p2>p3
(5)α1+α3=<1.
8.某温度下,在定容的密闭容器中,建立了如下平衡:2NO2(g)?N2O4(g),若再向容器中通入一定量的NO2气体或N2O4气体,重新达到平衡后,容器内NO2气体质量分数比原平衡时( )
| A. | 都增大 | B. | 前者增大,后者减小 | ||
| C. | 都减小 | D. | 前者减小,后者增大 |
7.在5L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)×c(H{\;}_{2}O)}{c(CO{\;}_{2})×c({H}_{2})}$.
(2)该反应的△H>(填“>”或“<”)0.
(3)某温度下,该反应平衡时各物质的浓度关系为:3[c(CO2)•c(H2)]=5[c(CO)•c(H2O)],则反应温度是700℃.
(4)将CO2和H2各0.05mol充入该容器中,某温度下达到平衡状态,测得c(CO)=0.008mol/L,则CO2的转化率为80%.
(5)若容器容积不变,温度不变,平衡后向容器内继续充入CO2,则H2的转化率变大,CO2的转化率变小(填“变大”“变小”或“不变”).
(6)该反应达到平衡后,只改变一个条件,平衡向逆反应方向移动的是ad.
a.降低温度 b.保持压强不变,充入N2 c.保持容器容积不变,充入N2 d.保持容器容积不变,加入NaOH溶液.
0 173589 173597 173603 173607 173613 173615 173619 173625 173627 173633 173639 173643 173645 173649 173655 173657 173663 173667 173669 173673 173675 173679 173681 173683 173684 173685 173687 173688 173689 173691 173693 173697 173699 173703 173705 173709 173715 173717 173723 173727 173729 173733 173739 173745 173747 173753 173757 173759 173765 173769 173775 173783 203614
| t/℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)该反应的△H>(填“>”或“<”)0.
(3)某温度下,该反应平衡时各物质的浓度关系为:3[c(CO2)•c(H2)]=5[c(CO)•c(H2O)],则反应温度是700℃.
(4)将CO2和H2各0.05mol充入该容器中,某温度下达到平衡状态,测得c(CO)=0.008mol/L,则CO2的转化率为80%.
(5)若容器容积不变,温度不变,平衡后向容器内继续充入CO2,则H2的转化率变大,CO2的转化率变小(填“变大”“变小”或“不变”).
(6)该反应达到平衡后,只改变一个条件,平衡向逆反应方向移动的是ad.
a.降低温度 b.保持压强不变,充入N2 c.保持容器容积不变,充入N2 d.保持容器容积不变,加入NaOH溶液.