14.在MgCl2、KCl、K2SO4三种盐的混合溶液中含有0.8mol K+、0.1mol Mg2+、0.4mol Cl-,则该溶液中含SO${\;}_{4}^{2-}$为( )
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3mol | D. | 0.15 mol |
13.实验中需1mol•L-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是( )
| A. | 1000 mL,106.0g | B. | 950 mL,100.7g | C. | 950 mL,106.0g | D. | 1000 mL,100.7 g |
12.下列离子方程式正确的是( )
| A. | 硝酸银溶液与铜反应:Cu+Ag+═Cu2++Ag | |
| B. | 氧化镁与盐酸反应:O2-+2H+═H2O | |
| C. | 碳酸钙与盐酸反应:CO${\;}_{3}^{2-}$+2H+═H2O+CO2↑ | |
| D. | Fe(OH)3加入H2SO4溶液中:3H++Fe(OH)3═Fe3++3H2O |
11.下列有关氧化还原反应的叙述正确的是( )
| A. | 金属单质在氧化还原反应中只能作还原剂,非金属单质只能作氧化剂 | |
| B. | 化合物中某元素处于最低价只能被还原 | |
| C. | 失电子越容易的还原剂,其还原性越强 | |
| D. | 某元素在反应中由化合物转化为单质,该元素一定被氧化 |
10.已知氨水的密度小于水的密度,将质量分数分别为80%和20%的氨水等体积混合,混合后的质量分数为( )
| A. | 大于50% | B. | 小于50% | C. | 等于50% | D. | 不能确定 |
9.下列说法或操作,其中正确的是( )
①配制一定物质的量浓度的溶液时将洗涤液直接倒入容量瓶
②用托盘天平称量25.28g KCl
③用酒精可以从饱和碘水中萃取碘
④让一束光通过胶体,从通过光线的方向可以看到一条光亮的“通路”
⑤从含有少量氯化钠的硝酸钾溶液中提取硝酸钾可用结晶的方法.
①配制一定物质的量浓度的溶液时将洗涤液直接倒入容量瓶
②用托盘天平称量25.28g KCl
③用酒精可以从饱和碘水中萃取碘
④让一束光通过胶体,从通过光线的方向可以看到一条光亮的“通路”
⑤从含有少量氯化钠的硝酸钾溶液中提取硝酸钾可用结晶的方法.
| A. | ①②③④⑤ | B. | ②④⑤ | C. | ④⑤ | D. | ⑤ |
8.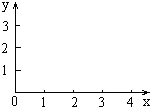 将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.
将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.
 将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.
将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0).若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在图中画出函数图象.| x值 | y=f(x) |
| 0<x≤3 | y=$\frac{2}{3}$x |
| 3<x<3.2 | y=32-10x |
| - | - |
| - | - |
7.已知:相同的两种元素组成的四种微粒A、B、C、D的质子数依次增多,A、B、C、D的电子数如表(A、B、C、D有两组可能),且D中的电子数等于质子数,D1可作医用消毒液. 其中B1的沸点比B2高.
试回答下列问题:
(1)上述两组八种微粒的组成元素中,原子序数处在中间的元素在元素周期表的位置是第二周期第VA族; D1的电子式为: .
.
(2)液态的B2与Na反应的方程式:2Na+2NH3(l)=2NaNH2+H2↑.
(3)①亚氯酸钠(NaClO2)主要可用于棉纺、造纸业做漂白剂,也用于食品消毒、水处理等,制备亚氯酸钠,可以将ClO2气体通入D1和NaOH的混合液中,请写出制备方程式2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2,其中D1的作用是还原剂;
②利用①中原理制备出NaClO2•3H2O晶体的试样,可以用“间接碘量法”测定试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下(已知:I2+2S2O32-=S4O62-+2I-):
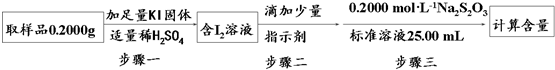
步骤一的离子方程式为ClO2-+4I-+4H+=2I2+Cl-+2H2O;步骤二的指示剂是淀粉;步骤三中出现溶液由蓝色变无色,且半分钟不变色现象现象时,达到滴定终点;计算该试样中NaClO2•3H2O的质量百分数为90.3%.
| ① | A1 | B1 | C1 | D1 |
| 电子数 | 10 | 10 | 10 | 18 |
| ② | A2 | B2 | C2 | D2 |
| 电子数 | 10 | 10 | 10 | 18 |
(1)上述两组八种微粒的组成元素中,原子序数处在中间的元素在元素周期表的位置是第二周期第VA族; D1的电子式为:
 .
.(2)液态的B2与Na反应的方程式:2Na+2NH3(l)=2NaNH2+H2↑.
(3)①亚氯酸钠(NaClO2)主要可用于棉纺、造纸业做漂白剂,也用于食品消毒、水处理等,制备亚氯酸钠,可以将ClO2气体通入D1和NaOH的混合液中,请写出制备方程式2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2,其中D1的作用是还原剂;
②利用①中原理制备出NaClO2•3H2O晶体的试样,可以用“间接碘量法”测定试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下(已知:I2+2S2O32-=S4O62-+2I-):

步骤一的离子方程式为ClO2-+4I-+4H+=2I2+Cl-+2H2O;步骤二的指示剂是淀粉;步骤三中出现溶液由蓝色变无色,且半分钟不变色现象现象时,达到滴定终点;计算该试样中NaClO2•3H2O的质量百分数为90.3%.
5.下列离子反应方程式正确的是( )
0 173099 173107 173113 173117 173123 173125 173129 173135 173137 173143 173149 173153 173155 173159 173165 173167 173173 173177 173179 173183 173185 173189 173191 173193 173194 173195 173197 173198 173199 173201 173203 173207 173209 173213 173215 173219 173225 173227 173233 173237 173239 173243 173249 173255 173257 173263 173267 173269 173275 173279 173285 173293 203614
| A. | 在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O | |
| B. | 向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O═2HCO3- | |
| C. | 将氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| D. | 向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:Al3++SO42-+Ba2++3OH-═BaSO4↓+Al(OH)3↓ |