3.下列化学用语的表达正确的是( )
| A. | NaHSO3在溶液中的电离:NaHSO3=Na++H++SO32- | |
| B. | Cl-的结构示意图: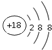 | |
| C. | HClO结构式:H-Cl-O | |
| D. | 医用钡餐的化学式:BaSO4 |
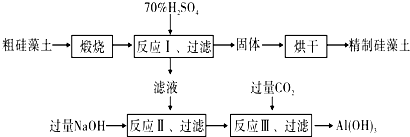
2.硅藻土是一种硅质岩石,主要分布在中国、美国等国.它主要由古代硅藻的遗骸所组成.其化学成分以SiO2为主,可用SiO2•nH2O表示,并含有少量的有机质、Al2O3、Fe2O3和MgO等杂质.如图是生产精制硅藻土并获得Al(OH)3的工艺流程.
(1)该工艺流程中多处涉及到过滤操作,其需要用到的玻璃仪器主要有烧杯、玻璃棒、(普通)漏斗.
(2)假设所得反应Ⅰ的滤液中各种金属阳离子的浓度均为0.001mol/L( 查数据可知部分难溶物的溶度积Ksp数值如下表所示(25℃))
①由数据分析可知,向反应Ⅰ的滤液中逐滴加入NaOH溶液,金属阳离子的沉淀顺序依次为:Fe3+>Al3+>Mg2+.(用“离子符号”回答)
②当Fe3+恰好沉淀完全时溶液的PH值为3.3.(已知:lg2=0.3)
(3)反应Ⅲ中生成Al(OH)3沉淀的离子方程式是AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓.
(4)实验室用酸碱滴定法测定硅藻土中硅含量的步骤如下:
步骤1:准确称取样品a g,加入适量KOH固体,在高温下充分灼烧,冷却,加水溶解.
步骤2:将所得溶液完全转移至塑料烧杯中,加入硝酸至强酸性,得硅酸浊液.
步骤3:向硅酸浊液中加入NH4F溶液、饱和KCl溶液,得K2SiF6沉淀,用塑料漏斗过滤并洗涤.
步骤4:将K2SiF6转移至另一烧杯中,加入一定量蒸馏水,采用70℃水浴加热使其充分水解(K2SiF6+3H2O=H2SiO3+4HF+2KF).
步骤5:向上述水解液中加入数滴酚酞,趁热用浓度为c mol/L NaOH的标准溶液滴定至终点,消耗NaOH标准溶液V mL.
①步骤3中采用饱和KCl溶液洗涤沉淀,其目的是洗去沉淀表面的HF等杂质;增大K+浓度,减少K2SiF6的损失.
②步骤5中判断滴定终点的现象是最后一滴滴入后溶液由无色变为粉红色,且30s不褪色.
③已知样品中SiO2的质量分数可用公式“w(SiO2)=$\frac{15cV×1{0}^{-3}}{a}$×100%”进行计算.
由此分析步骤5中与NaOH标准溶液发生中和反应的酸为B.
A.H2SiO3 B.HF C.H2SiO3和HF D.无法确定
(1)该工艺流程中多处涉及到过滤操作,其需要用到的玻璃仪器主要有烧杯、玻璃棒、(普通)漏斗.
(2)假设所得反应Ⅰ的滤液中各种金属阳离子的浓度均为0.001mol/L( 查数据可知部分难溶物的溶度积Ksp数值如下表所示(25℃))
| 难溶物 | 溶度积Ksp |
| Mg(OH)2 | 1.8×10-11 |
| Al(OH)3 | 1.0×10-33 |
| Fe(OH)3 | 8.0×10-38 |
②当Fe3+恰好沉淀完全时溶液的PH值为3.3.(已知:lg2=0.3)
(3)反应Ⅲ中生成Al(OH)3沉淀的离子方程式是AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓.
(4)实验室用酸碱滴定法测定硅藻土中硅含量的步骤如下:
步骤1:准确称取样品a g,加入适量KOH固体,在高温下充分灼烧,冷却,加水溶解.
步骤2:将所得溶液完全转移至塑料烧杯中,加入硝酸至强酸性,得硅酸浊液.
步骤3:向硅酸浊液中加入NH4F溶液、饱和KCl溶液,得K2SiF6沉淀,用塑料漏斗过滤并洗涤.
步骤4:将K2SiF6转移至另一烧杯中,加入一定量蒸馏水,采用70℃水浴加热使其充分水解(K2SiF6+3H2O=H2SiO3+4HF+2KF).
步骤5:向上述水解液中加入数滴酚酞,趁热用浓度为c mol/L NaOH的标准溶液滴定至终点,消耗NaOH标准溶液V mL.
①步骤3中采用饱和KCl溶液洗涤沉淀,其目的是洗去沉淀表面的HF等杂质;增大K+浓度,减少K2SiF6的损失.
②步骤5中判断滴定终点的现象是最后一滴滴入后溶液由无色变为粉红色,且30s不褪色.
③已知样品中SiO2的质量分数可用公式“w(SiO2)=$\frac{15cV×1{0}^{-3}}{a}$×100%”进行计算.
由此分析步骤5中与NaOH标准溶液发生中和反应的酸为B.
A.H2SiO3 B.HF C.H2SiO3和HF D.无法确定

1. 乙二酸( HOOC-COOH)俗称草酸,它广泛分布于植物的茎叶中.为了探究乙二酸的性质.某化学兴趣小组设计了如下实验,试根据所给信息,回答有关问题:
乙二酸( HOOC-COOH)俗称草酸,它广泛分布于植物的茎叶中.为了探究乙二酸的性质.某化学兴趣小组设计了如下实验,试根据所给信息,回答有关问题:
I.乙二酸的弱酸性:
查数据可知(25℃):
(1)H2C2O4的电离方程式为H2C2O4?H++HC2O4-、HC2O4-?H++C2O42-.
(2)向盛有饱和NaHCO3溶液的试管里加入少量草酸溶液,可观察到有无色气泡产生,该反应的离子方程式为2HCO3-+H2C2O4=C2O42-+2H2O+2CO2↑.
(3)该小组同学将0.1mol•L-1草酸溶液和0.1mol•L-1的NaOH等体积混合后,测定反应后溶液呈酸性,则所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
(4)为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是AD.
A.测0.1mol•L-1草酸溶液的pH B.将草酸溶液加入Na2CO3溶液中,有CO2放出
C.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色 D.测草酸钠溶液的pH
Ⅱ.一定温度下,草酸晶体加水稀释过程中溶液的导电能力曲线如图所示:
(1)下列有关草酸稀释的说法正确的是A
A.a、b、c三点草酸的电离程度:a<b<c
B.a、b、c三点溶液的pH:c<a<b
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏大
D.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b
(2)在上述稀释过程中,始终保持增大趋势的是BD
A.溶液PH值 B.草酸电离度α C.c(H+)•c(OH-) D.C2O42-个数
Ⅲ.已知草酸的钠盐和钾盐易溶于水,而其钙盐却难溶于水.查数据可知:CaCO3、CaC2O4的溶度积常数Ksp(25℃)分别为5.0×10-9、2.5×10-9,向0.6mol•L-1Na2C2O4溶液中加入过量CaCO3固体后,溶液中的c(CO32-)=0.4mol/L.
 乙二酸( HOOC-COOH)俗称草酸,它广泛分布于植物的茎叶中.为了探究乙二酸的性质.某化学兴趣小组设计了如下实验,试根据所给信息,回答有关问题:
乙二酸( HOOC-COOH)俗称草酸,它广泛分布于植物的茎叶中.为了探究乙二酸的性质.某化学兴趣小组设计了如下实验,试根据所给信息,回答有关问题:I.乙二酸的弱酸性:
查数据可知(25℃):
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
| H2CO3 (碳酸) | K1=4.4×10-7 | H2C2O4 (草酸) | K1=5.4×10-2 |
| K2=4.7×10-11 | K2=5.4×10-5 |
(2)向盛有饱和NaHCO3溶液的试管里加入少量草酸溶液,可观察到有无色气泡产生,该反应的离子方程式为2HCO3-+H2C2O4=C2O42-+2H2O+2CO2↑.
(3)该小组同学将0.1mol•L-1草酸溶液和0.1mol•L-1的NaOH等体积混合后,测定反应后溶液呈酸性,则所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
(4)为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是AD.
A.测0.1mol•L-1草酸溶液的pH B.将草酸溶液加入Na2CO3溶液中,有CO2放出
C.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色 D.测草酸钠溶液的pH
Ⅱ.一定温度下,草酸晶体加水稀释过程中溶液的导电能力曲线如图所示:
(1)下列有关草酸稀释的说法正确的是A
A.a、b、c三点草酸的电离程度:a<b<c
B.a、b、c三点溶液的pH:c<a<b
C.用湿润的pH试纸测量a处溶液的pH,测量结果偏大
D.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b
(2)在上述稀释过程中,始终保持增大趋势的是BD
A.溶液PH值 B.草酸电离度α C.c(H+)•c(OH-) D.C2O42-个数
Ⅲ.已知草酸的钠盐和钾盐易溶于水,而其钙盐却难溶于水.查数据可知:CaCO3、CaC2O4的溶度积常数Ksp(25℃)分别为5.0×10-9、2.5×10-9,向0.6mol•L-1Na2C2O4溶液中加入过量CaCO3固体后,溶液中的c(CO32-)=0.4mol/L.
20.一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g),进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3h):
请回答下列问题:
(1)该反应的平衡常数表达式为$\frac{[N{H}_{3}]^{2}×[{O}_{2}]^{\frac{3}{2}}}{[{N}_{2}]×[{H}_{2}O]^{3}}$.
(2)已知在所给条件下投入1molN2和3molH2O(l),当反应达到平衡时消耗了35kJ的热量,并收集到0.4molNH3.则N2的平衡转化率为20%,该反应的热化学方程式可表示为N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g)△H=+175.0kJ•mol-1.
(3)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢,请提出可提高其反应速率同时增大NH3生成量的措施升高温度、增大氮气浓度.(列出两种即可)
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ•mol-1.在某体积为10L的恒温恒容密闭容器中加入2mol N2和4mol H2,2min后反应达到平衡时容器内的压强是起始压强的2/3.求:
①2min内NH3的反应速率υ(NH3)=0.1 mol/(L•min).
②下列有关该化学反应的说法正确的是B(填字母序号).
A.在恒温恒压条件下,向上述平衡体系中通入少量氩气,平衡不移动
B.在恒温恒容条件下,向上述平衡体系中通入少量氩气,平衡不移动
C.实际工业生产中为提高H2的转化率,通常通入过量的N2,且N2过量越多越好
D.当温度、体积相同且恒定不变时,向甲容器中通入0.5mol N2和1.5mol H2,乙容器中通入1mol N2和3molH2,后者反应放出的热量为前者的两倍.
| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
(1)该反应的平衡常数表达式为$\frac{[N{H}_{3}]^{2}×[{O}_{2}]^{\frac{3}{2}}}{[{N}_{2}]×[{H}_{2}O]^{3}}$.
(2)已知在所给条件下投入1molN2和3molH2O(l),当反应达到平衡时消耗了35kJ的热量,并收集到0.4molNH3.则N2的平衡转化率为20%,该反应的热化学方程式可表示为N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g)△H=+175.0kJ•mol-1.
(3)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢,请提出可提高其反应速率同时增大NH3生成量的措施升高温度、增大氮气浓度.(列出两种即可)
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ•mol-1.在某体积为10L的恒温恒容密闭容器中加入2mol N2和4mol H2,2min后反应达到平衡时容器内的压强是起始压强的2/3.求:
①2min内NH3的反应速率υ(NH3)=0.1 mol/(L•min).
②下列有关该化学反应的说法正确的是B(填字母序号).
A.在恒温恒压条件下,向上述平衡体系中通入少量氩气,平衡不移动
B.在恒温恒容条件下,向上述平衡体系中通入少量氩气,平衡不移动
C.实际工业生产中为提高H2的转化率,通常通入过量的N2,且N2过量越多越好
D.当温度、体积相同且恒定不变时,向甲容器中通入0.5mol N2和1.5mol H2,乙容器中通入1mol N2和3molH2,后者反应放出的热量为前者的两倍.
19.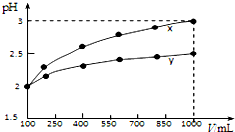 有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )
有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )
 有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )
有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )| A. | 稀释前x、y的物质的量浓度相等 | B. | 相同温度下,电离常数Ka(x)>Ka(y) | ||
| C. | 随着稀释的进行,y的电离程度减小 | D. | 稀释相同倍数后的溶液中c(H+):x>y |
18.现有四种溶液:①0.01mol/L HCl溶液 ②PH=2的CH3COOH溶液 ③PH=12的NaOH溶液 ④0.01mol/LNH3•H2O溶液,下列有关四种溶液的说法中不正确的是( )
| A. | 水的电离程度:①=②=③<④ | B. | 与相同Zn粒反应平均速率:①<② | ||
| C. | 溶液PH值:①=②<③<④ | D. | 稀释相同的倍数所得溶液PH值:③>④ |
17.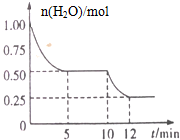 在2L密闭容器中进行反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H>0测得n(H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
在2L密闭容器中进行反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H>0测得n(H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
 在2L密闭容器中进行反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H>0测得n(H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )
在2L密闭容器中进行反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H>0测得n(H2O)随反应时间(t)的变化如图所示.下列判断正确的是( )| A. | 该反应的化学平衡常数表达式为K=c4(H2O)/c4(H2) | |
| B. | 5min时该反应的υ(正)等于9min时的υ(逆) | |
| C. | 0~5min内,υ(H2)=0.10mol/(L•min) | |
| D. | 10min时平衡发生移动可能是投入还原性铁粉引起 |
16.下列关于自发反应的叙述中,正确的是( )
| A. | 凡是放热反应都是自发的,凡是吸热反应都是非自发的 | |
| B. | 自发反应是无需外界条件就能自发进行的化学反应 | |
| C. | 在通常情况下,冰能自行融化,所以它是自发反应 | |
| D. | 由反应CaCO3(s)=CaO(s)+CO2(g)的特点分析可知其在高温下才能自发进行 |
15.常温下,在饱和Na2CO3溶液中下列关系正确的是( )
| A. | 2c(H2CO3 )+c(H +)+c(HCO3-)=c(OH -) | B. | c(CO32-)+c(HCO3-)+c(H2CO 3)=2 c(Na+) | ||
| C. | 2c(CO32-)+c(HCO3-)=c(H +)+c(Na+) | D. | c(Na+)>c(CO32-)>c(HCO3-)>c(OH -)>c(H+) |
14.下列关于工业生产的说法正确的是( )
0 172983 172991 172997 173001 173007 173009 173013 173019 173021 173027 173033 173037 173039 173043 173049 173051 173057 173061 173063 173067 173069 173073 173075 173077 173078 173079 173081 173082 173083 173085 173087 173091 173093 173097 173099 173103 173109 173111 173117 173121 173123 173127 173133 173139 173141 173147 173151 173153 173159 173163 173169 173177 203614
| A. | 工业生产中催化剂被大量使用是因为催化剂可以提高反应速率和转化率 | |
| B. | 合成氨的工业生产需在高温、高压和催化剂条件下进行是因为该反应是吸热反应 | |
| C. | 合成氨的工业生产中,及时将NH3液化分离出来将有利于提高生成物的产量 | |
| D. | 硫酸的工业生产中,SO2的催化氧化没有采用高压是因为压强对该反应无影响 |