3.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 12g石墨和C60的混合固体中,含NA个碳原子 | |
| B. | 标准状况下,2.24L水中含有0.1NA个水分子 | |
| C. | 7.8g过氧化钠含有的阴离子数为0.2NA | |
| D. | 0.1mol铁在足量氯气中燃烧,电子转移数目为0.2NA |
2.用化学平衡移动的知识分析:25℃时,50mL 0.1mol/L醋酸溶液中,若分别如下改变,对平衡有何影响?(完成表格)
| 改变条件 | 平衡移动方向 | n(H+) | c(H+) | c(CH3COO-) |
| 加入少量的醋酸钠固体 | ||||
| 加入镁条 | ||||
| 加入一定量水稀释 | ||||
| 加入一定量水稀释 | ||||
| 加入浓盐酸 | ||||
| 加入NaOH 固体 |
17.一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(保持温度不变),下列说法正确的是( )

0 172891 172899 172905 172909 172915 172917 172921 172927 172929 172935 172941 172945 172947 172951 172957 172959 172965 172969 172971 172975 172977 172981 172983 172985 172986 172987 172989 172990 172991 172993 172995 172999 173001 173005 173007 173011 173017 173019 173025 173029 173031 173035 173041 173047 173049 173055 173059 173061 173067 173071 173077 173085 203614

| A. | 右边CO与CO2分子数之比为3:1 | |
| B. | 右侧CO的质量为2.75g | |
| C. | 右侧气体密度是相同条件下氧气密度的16倍 | |
| D. | 若改变右边CO和CO2的充入量而使隔板处于距离右端1/6处,保持温度不变,则前后两次充入情况容器内的压强之比为24:25 |

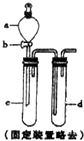 某兴趣小组采用如图装置制取并探究SO2气体的性质.
某兴趣小组采用如图装置制取并探究SO2气体的性质.
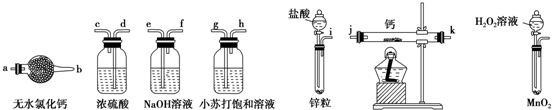
 .
.