9.下列物质属于氧化物的是( )
| A. | O2 | B. | CO | C. | KClO3 | D. | CH3COOH |
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在1L 2 mol/L的硝酸钙溶液中含有的硝酸根离子的数目为NA | |
| B. | 标准状况下22.4L乙醇完全燃烧,生成的二氧化碳的分子数为2NA | |
| C. | 46g二氧化氮(NO2)和46g四氧化二氮(N2O4)含有的原子数均为3NA | |
| D. | 1mol氢氧根离子中含有的电子数为9NA |
5.如图所示的家庭小实验中,主要发生物理变化的是( )
| A. | 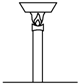 生成炭黑的实验 | B. |  净水 | ||
| C. | 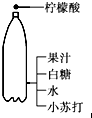 自制汽水 | D. | 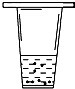 将鸡蛋壳放入醋中 |
4.短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
| A. | B与A只能组成BA3化合物 | |
| B. | 第三周期中,D原子的原子半径最大 | |
| C. | A、B、C三元素不可能形成离子化合物 | |
| D. | E的氧化物对应水化物一定有强的氧化性 |
3.下列溶液,加热后颜色一定变浅的是( )
| A. | 稀氨水和酚酞溶液 | B. | 滴有酚酞的Na2CO3溶液 | ||
| C. | 滴有酚酞的氢氧化钙溶液 | D. | 溶有SO2的品红溶液 |
2. 如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )
如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )
 如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )
如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )| A. | 盐酸、碳酸钠溶液、氢氧化钠溶液 | |
| B. | 氯化钠溶液、澄清石灰水、氢氧化钠溶液 | |
| C. | 盐酸、碳酸钠溶液、澄清石灰水 | |
| D. | 氢氧化钙溶液、盐酸、硫酸钠溶液 |
1.下列各组物质的溶液混合,如果其中酸过量时,仍有沉淀生成的是( )
| A. | NaOH、FeCl3、H2SO4 | B. | HCl、K2CO3、BaCl2 | ||
| C. | CuSO4、HCl、KOH | D. | BaCl2、HNO3、AgNO3 |
20. 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X可能是( )
①盐酸、Na2CO3溶液
②Cl2、Fe
③CO2、Ca(OH)2溶液
④NaOH溶液、AlCl3溶液
⑤偏铝酸钠溶液、盐酸
⑥氯化钙溶液、CO2
⑦钠、氧气.
0 172555 172563 172569 172573 172579 172581 172585 172591 172593 172599 172605 172609 172611 172615 172621 172623 172629 172633 172635 172639 172641 172645 172647 172649 172650 172651 172653 172654 172655 172657 172659 172663 172665 172669 172671 172675 172681 172683 172689 172693 172695 172699 172705 172711 172713 172719 172723 172725 172731 172735 172741 172749 203614
 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X可能是( )①盐酸、Na2CO3溶液
②Cl2、Fe
③CO2、Ca(OH)2溶液
④NaOH溶液、AlCl3溶液
⑤偏铝酸钠溶液、盐酸
⑥氯化钙溶液、CO2
⑦钠、氧气.
| A. | ①②③④ | B. | ①③④⑤ | C. | ③④⑤⑦ | D. | ③④⑤⑥ |
 CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为-24.2℃,20℃时在水中的溶解度为400mL,易溶于乙醇和丙醇等有机溶剂.
CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为-24.2℃,20℃时在水中的溶解度为400mL,易溶于乙醇和丙醇等有机溶剂.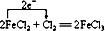 .
.