9.某实验小组用0.50mol•L-1 NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
Ⅰ.配制0.50mol•L-1 NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母):a b e.
Ⅱ.某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀.甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH)2的混合物,他们设计实验测定沉淀中CuCO3的质量分数.
(1)按照甲同学的观点,发生反应的离子方程式为Cu2++2HCO3=CuCO3↓+CO2↑+H2O.
(2)两同学利用如图所示装置进行测定:

①在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为过滤、洗涤、干燥.
②装置E中碱石灰的作用是防止空气中CO2和水蒸气进入装置D.
③实验过程中有以下操作步骤:
a.关闭K1、K3,打开K2、K4,充分反应
b.打开K1、K4,关闭K2、K3,通入过量空气
c.打开K1、K3,关闭K2、K4,通入过量空气
正确的顺序是cab(填选项序号,下同).若未进行步骤b,将使测量结果偏低.
④若沉淀样品质量为m g,装置D质量增加了n g,则沉淀中CuCO3的质量分数为$\frac{31n}{11m}$.
(3)丙同学认为还可以通过测量CO2的体积或测量样品质量和样品充分灼烧后的质量来测定沉淀中CuCO3的质量分数.
Ⅰ.配制0.50mol•L-1 NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母):a b e.
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
(1)按照甲同学的观点,发生反应的离子方程式为Cu2++2HCO3=CuCO3↓+CO2↑+H2O.
(2)两同学利用如图所示装置进行测定:

①在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为过滤、洗涤、干燥.
②装置E中碱石灰的作用是防止空气中CO2和水蒸气进入装置D.
③实验过程中有以下操作步骤:
a.关闭K1、K3,打开K2、K4,充分反应
b.打开K1、K4,关闭K2、K3,通入过量空气
c.打开K1、K3,关闭K2、K4,通入过量空气
正确的顺序是cab(填选项序号,下同).若未进行步骤b,将使测量结果偏低.
④若沉淀样品质量为m g,装置D质量增加了n g,则沉淀中CuCO3的质量分数为$\frac{31n}{11m}$.
(3)丙同学认为还可以通过测量CO2的体积或测量样品质量和样品充分灼烧后的质量来测定沉淀中CuCO3的质量分数.
6.下列离子方程式书写正确的是( )
| A. | 碳酸氢钙溶液中加入少量的氢氧化钠溶液Ca++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 氯气通入氢氧化钠溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O | |
| C. | 次氯酸钠溶液中通入过量CO2:2ClO-+CO2+H2O═CO32-+2HClO | |
| D. | 氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
3.能正确表示下列反应的离子方程式是( )
| A. | 向NaOH溶液中通入过量的CO2:CO2+OH-═HCO3- | |
| B. | 将SO2气体通入Ba(NO3)2溶液:SO2+H2O+Ba2+═BaSO3↓+2H+ | |
| C. | 实验室制氯气:MnO2+4HCl(浓)═Mn2++2Cl2↑+2H2O | |
| D. | AlCl3溶液与过量氨水混合:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
2.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 某溶液中加入氢氧化钠溶液生成蓝色沉淀,一定有Cu2+ |
1.使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏
低的是( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
0 172346 172354 172360 172364 172370 172372 172376 172382 172384 172390 172396 172400 172402 172406 172412 172414 172420 172424 172426 172430 172432 172436 172438 172440 172441 172442 172444 172445 172446 172448 172450 172454 172456 172460 172462 172466 172472 172474 172480 172484 172486 172490 172496 172502 172504 172510 172514 172516 172522 172526 172532 172540 203614
低的是( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
| A. | ①②⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ②③④ |
 直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.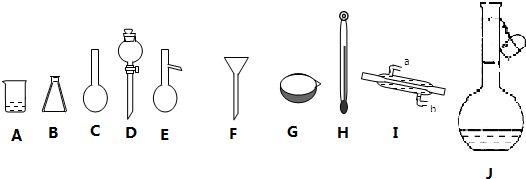
 ,NaClO属于离子(离子、共价)化合物.
,NaClO属于离子(离子、共价)化合物.



