17.为分别验证温度、浓度、催化剂颗粒大小对化学反应速率的影响规律,某同学设计了如下4组实验.
(1)上表中,反应速率最快的是实验2(填实验编号).
(2)实验3、4预期可得出的结论是催化剂颗粒越小,化学反应速率越大.
(3)设计实验2、3的目的是探究浓度对化学反应速率的影响.
(4)设计一个实验证明在其他条件相同时,改变温度对过氧化氢分解速率的影响(写出操作步骤):取相同浓度的过氧化氢溶液,控制催化剂相同,分别在在不同温度下加热,观察产生气体的快慢.
| 实验序号 | 温度 /℃ | H2O2溶液 初始浓度/% | MnO2 颗粒大小 |
| 1 | 25 | 4 | 无MnO2 |
| 2 | 25 | 12 | 1g细颗粒MnO2 |
| 3 | 25 | 4 | 1g细颗粒MnO2 |
| 4 | 25 | 4 | 1g粗颗粒MnO2 |
(2)实验3、4预期可得出的结论是催化剂颗粒越小,化学反应速率越大.
(3)设计实验2、3的目的是探究浓度对化学反应速率的影响.
(4)设计一个实验证明在其他条件相同时,改变温度对过氧化氢分解速率的影响(写出操作步骤):取相同浓度的过氧化氢溶液,控制催化剂相同,分别在在不同温度下加热,观察产生气体的快慢.
15.下列变化属于吸热过程的是( )
| A. | 天然气燃烧 | B. | 浓硫酸溶于水 | ||
| C. | CaO与水反应 | D. | B a(OH)2晶体与NH4Cl反应 |
14.已知OH-(aq)+H+(aq)═H2O(l);△H=-57.3kJ/mol,下列说法中正确的是( )
| A. | 浓硫酸和NaOH溶液反应,生成 lmol水时放热57.3kJ | |
| B. | 含lmolH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57 kJ | |
| C. | 1L0.lmol/L CH3COOH与1L0.lmol/L NaOH溶液反应后放热为5.73kJ | |
| D. | 1L0.lmol/L HNO3与 1L0.lmol/L NaOH溶液反应后放热为 5.73kJ |
12.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
| B | 向稀的苯酚水溶液中滴加饱 和溴水 | 生成白色沉淀 | 产物三溴苯酚溶于水 |
| C | 向含I-的无色溶液中滴加少量铁盐溶液,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Fe3+>I2 |
| D | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法不正确的是( )
| A. | 1mol氢 | B. | 1mol氧原子 | C. | 1molH | D. | 1molNaOH |
8.下列叙述正确的是( )
0 172165 172173 172179 172183 172189 172191 172195 172201 172203 172209 172215 172219 172221 172225 172231 172233 172239 172243 172245 172249 172251 172255 172257 172259 172260 172261 172263 172264 172265 172267 172269 172273 172275 172279 172281 172285 172291 172293 172299 172303 172305 172309 172315 172321 172323 172329 172333 172335 172341 172345 172351 172359 203614
| A. | 摩尔质量就等于该物质的相对分子质量或相对原子质量 | |
| B. | 硫酸的摩尔质量是98克 | |
| C. | 1molH2O的质量为18克 | |
| D. | 2molH2O的质量为18克 |
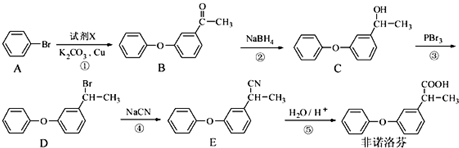
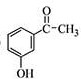 .
.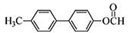 .
.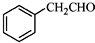 为原料制备
为原料制备 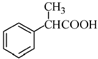 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH$→_{浓硫酸△}^{CH_{3}COOH}$CH3COOCH2CH3合成路线流程图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH$→_{浓硫酸△}^{CH_{3}COOH}$CH3COOCH2CH3合成路线流程图: .
.