18.我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法.
I.已知反应$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)△H=-23.5kJ•mol-1,该反应在1000℃的平衡常数等于4.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡.
(1)CO的平衡转化率=60%
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是d.
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:

(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=0.15mol/(L•min).
(4)已知氢气的燃烧热286kJ/mol,请写出甲醇气体不充分燃烧的热化学方程式CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol.
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
则下列关系正确的是ADE
A.c1=c2B.2Q1=Q3C.2α1=α3D.α1+α2=1E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量.
I.已知反应$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)△H=-23.5kJ•mol-1,该反应在1000℃的平衡常数等于4.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡.
(1)CO的平衡转化率=60%
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是d.
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:

(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=0.15mol/(L•min).
(4)已知氢气的燃烧热286kJ/mol,请写出甲醇气体不充分燃烧的热化学方程式CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol.
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
A.c1=c2B.2Q1=Q3C.2α1=α3D.α1+α2=1E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量.
17.在恒温条件下,向盛有食盐的2L恒容密闭容器中加入0.2molNO2,0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g)△H1<0 平衡常数K1
②2NO(g)+Cl2(g)═2ClNO(g)△H2<0 平衡常数K2
10min时反应达到平衡,测得容器内体系的压强减少20%,10min内用ClNO(g)表示的平均反应速率v(ClNO)═7.0×10-3mol•L•min-1.
下列说法正确的是( )
①2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g)△H1<0 平衡常数K1
②2NO(g)+Cl2(g)═2ClNO(g)△H2<0 平衡常数K2
10min时反应达到平衡,测得容器内体系的压强减少20%,10min内用ClNO(g)表示的平均反应速率v(ClNO)═7.0×10-3mol•L•min-1.
下列说法正确的是( )
| A. | 反应4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数$\frac{{{k}_{1}}^{2}}{{k}_{2}}$ | |
| B. | 平衡后c(Cl2)=2.5×10-2mol•L-1 | |
| C. | 其他条件保持不变,反应在恒压条件下进行,则平衡常数K2增大 | |
| D. | 平衡时NO2的转化率为50% |
16.在对应的温度下,体积均为2L的三个恒容密闭容器中发生如下可逆反应:N2O4(g)?2NO2(g)△H=+57kJ/mol,实验测得有关数据如下表:
下列叙述正确的是( )
| 容器编号 | 温度 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化 | 达到平衡所需时间 | |
| N2O4 | NO2 | ||||
| ① | T1 | 2 | 0 | 吸热22.8kJ | 2min |
| ② | T2 | 0 | 4 | 放热Q(Q>0)kJ | … |
| ③ | T3 | 3 | 1 | … | … |
| A. | 容器①中,从起始到平衡时,用NO2表示的平均反应速率v(NO2)为0.2mol(L•min) | |
| B. | 若容器①在恒温恒压下达平衡,该条件下的平衡常数等于0.2 | |
| C. | 若Q<34.2kJ,则T1>T2 | |
| D. | 容器③在达平衡前,v(正)<v(逆) |
15.在一定条件下CO(g)和H2(g)发生反应:CO(g)+2H2(g)?CH3OH(g).在容积固定且均为1L的a、b、c三个密闭容器中分别充入1mol CO(g)和2mol H2(g),三个容器的反应温度分别为T1、T2、T3(依次升高)且恒定不变,测得反应均进行到5min时CH3OH(g)的浓度如图所示.下列说法正确的是( )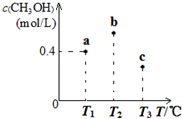

| A. | a容器中,0~5min内平均反应速率ν(H2)=0.04mol/(L.min) | |
| B. | 反应均进行到5min时,三个容器中一定达到化学平衡状态的是b | |
| C. | 当三个容器内的反应都达到化学平衡时,CO转化率最大的是a | |
| D. | 保持温度和容积不变,若开始时向b容器中充入0.6mol CO(g)、1.2mol H2(g)和0.4mol CH3OH(g),则反应开始时ν正(H2)<ν(逆) |
14. 一定温度下,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)△H,经过一段时间后达到平衡,反应过程中测定的部分数据如图.下列说法正确的是( )
一定温度下,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)△H,经过一段时间后达到平衡,反应过程中测定的部分数据如图.下列说法正确的是( )
 一定温度下,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)△H,经过一段时间后达到平衡,反应过程中测定的部分数据如图.下列说法正确的是( )
一定温度下,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)△H,经过一段时间后达到平衡,反应过程中测定的部分数据如图.下列说法正确的是( )| A. | 反应在50s~250s内的平均速率v(PCl3)=4.0×10-4mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl5)=0.38 mol•L-1,则反应的△H<0 | |
| C. | 保持其他条件不变,将容器的容积缩小一半,平衡逆向移动,化学平衡常数减小 | |
| D. | 相同温度下,起始时向容器中充入0.5 mol PCl5,重新达到平衡时,0.1 mol<n(PCl3)<0.2 mol |
13.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 该温度下此反应的平衡常数K=144 | |
| C. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 | |
| D. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) |
11.工业燃烧煤、石油等化石燃料释放出大量氨氧化物NO3、CO2、SO2等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用.
Ⅰ.脱硝:已知:H2的燃烧热为285.8kJ•mol-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H<0
(1)①下列叙述能说明此反应达到平衡状态的是de.
a.混合气体的平均摩尔质量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时有3molH-H键断裂
②CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t4CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见下表:
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(Ⅰ)<K(Ⅱ)(填“>”、“<”或“=”).
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=0.025mol/(L.min);;在反应Ⅰ的条件下,该反应的平衡常数为$\frac{4}{27}$
③对反应Ⅰ,在其它条件不变,若30min时只改变一个条件,此时H2的物质的量浓度为1.6mol/L,则该条件可能为减少CO2的浓度,增大甲醇或水蒸气浓度,或升高温度.(写出两个情况即可)
④对反应Ⅰ,若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
Ⅰ.脱硝:已知:H2的燃烧热为285.8kJ•mol-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H<0
(1)①下列叙述能说明此反应达到平衡状态的是de.
a.混合气体的平均摩尔质量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时有3molH-H键断裂
②CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t4CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见下表:
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ绝热恒容 | 0min | 0 | 0 | 2 | 2 |
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=0.025mol/(L.min);;在反应Ⅰ的条件下,该反应的平衡常数为$\frac{4}{27}$
③对反应Ⅰ,在其它条件不变,若30min时只改变一个条件,此时H2的物质的量浓度为1.6mol/L,则该条件可能为减少CO2的浓度,增大甲醇或水蒸气浓度,或升高温度.(写出两个情况即可)
④对反应Ⅰ,若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
9.700℃时,H2(g)+CO2(g)?H2O(g)+CO(g).该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示.其中甲经2min达平衡时,v(H2O)为0.025mol/(L•min),下列判断错误的是( )
0 172129 172137 172143 172147 172153 172155 172159 172165 172167 172173 172179 172183 172185 172189 172195 172197 172203 172207 172209 172213 172215 172219 172221 172223 172224 172225 172227 172228 172229 172231 172233 172237 172239 172243 172245 172249 172255 172257 172263 172267 172269 172273 172279 172285 172287 172293 172297 172299 172305 172309 172315 172323 203614
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.10 | 0.20 | 0.20 |
| c(CO2)/mol/L | 0.10 | 0.10 | 0.20 |
| A. | 平衡时,乙中CO2的转化率等于50% | |
| B. | 当反应平衡时,丙中c(CO2)是甲中的2倍 | |
| C. | 温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应 | |
| D. | 其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/LCO2,到达平衡时c (CO)与乙不同 |
 2Fe3O4(S)+C.
2Fe3O4(S)+C.
 .
.
 CO(NH2)2+H2O.开始以氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为40%.
CO(NH2)2+H2O.开始以氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为40%.