17.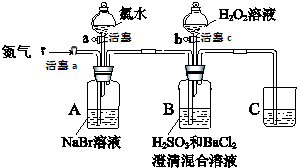 (某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)
(某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)
实验记录如下:
请回答下列问题:
(1)装置C的作用是吸收尾气中的SO2、Br2等,防止污染空气,C中盛放的药品是NaOH溶液.
(2)实验操作Ⅰ中,吹入氮气的目的是排尽装置内的空气,排除O2对氧化H2SO3实验的干扰.
(3)实验操作Ⅲ,B装置中发生反应的离子方程式是Br2+H2SO3+H2O═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓.
(4)实验操作Ⅳ,开始时颜色无明显变化的原因是(写出一条即可):H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可).
(5)实验操作Ⅳ,混合液逐渐变成红棕色,其对应的离子方程式H2O2+2Br-+2H+=Br2+2H2O.
(6)由上述实验得出的结论是氧化性:H2O2>Br2>H2SO3.
(7)实验操作Ⅴ的目的是确认实验III中吹出的气体中不含Cl2,排除Cl2对后续实验的干扰.
 (某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)
(某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)实验记录如下:
| 实验操作 | 实验现象 | |
| Ⅰ | 打开活塞a,通入一段时间氮气,关闭活塞a | 无明显实验现象 |
| Ⅱ | 打开活塞b,滴加氯水,关闭活塞b | A中溶液变为红棕色. |
| Ⅲ | 打开活塞a,吹入氮气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化. |
| Ⅳ | 停止吹入氮气,关闭活塞a;打开活塞c,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色. |
| Ⅴ | 打开活塞b,滴加氯水 | A中溶液变为红棕色. |
(1)装置C的作用是吸收尾气中的SO2、Br2等,防止污染空气,C中盛放的药品是NaOH溶液.
(2)实验操作Ⅰ中,吹入氮气的目的是排尽装置内的空气,排除O2对氧化H2SO3实验的干扰.
(3)实验操作Ⅲ,B装置中发生反应的离子方程式是Br2+H2SO3+H2O═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓.
(4)实验操作Ⅳ,开始时颜色无明显变化的原因是(写出一条即可):H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可).
(5)实验操作Ⅳ,混合液逐渐变成红棕色,其对应的离子方程式H2O2+2Br-+2H+=Br2+2H2O.
(6)由上述实验得出的结论是氧化性:H2O2>Br2>H2SO3.
(7)实验操作Ⅴ的目的是确认实验III中吹出的气体中不含Cl2,排除Cl2对后续实验的干扰.
15.研究PM 2.5、SO2、NOx等,对监测空气质量具有重要意义.取某样本用蒸馏水处理制成待测液,其中所含离子的化学组分及其浓度如下表:
请回答下列问题:
(1)NO3-中心原子的杂化类型是sp2,离子中所含大π键是π46.
(2)根据表中数据计算此待测液中c(H+)浓度a为1×10-4mol/L.
(3)NOx是汽车尾气中的主要污染物之一.
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有H+、NO3-.
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2═2NO,在汽车尾气系统中加装催化转化器可减少NOx的污染.
(4)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是CaSO4.
②吸收烟气中的SO2,以下物质可作吸收剂的是a(填序号),写出吸收SO2过程中发生的一个反应的离子方程式2OH-+SO2═SO32-+H2O或OH-+SO2═HSO3-.
a.NaOH b.H2SO4 c.NaHSO3.
| 离子 | K+ | Na+ | NH4+ | H+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
(1)NO3-中心原子的杂化类型是sp2,离子中所含大π键是π46.
(2)根据表中数据计算此待测液中c(H+)浓度a为1×10-4mol/L.
(3)NOx是汽车尾气中的主要污染物之一.
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有H+、NO3-.
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2═2NO,在汽车尾气系统中加装催化转化器可减少NOx的污染.
(4)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是CaSO4.
②吸收烟气中的SO2,以下物质可作吸收剂的是a(填序号),写出吸收SO2过程中发生的一个反应的离子方程式2OH-+SO2═SO32-+H2O或OH-+SO2═HSO3-.
a.NaOH b.H2SO4 c.NaHSO3.
14.下列物质的空间构型是平面三角形的是( )
| A. | NH3 | B. | BF3 | C. | PCl3 | D. | ClO3- |
13.为了确定(NH4)2Fe(SO4)2•6H2O(硫酸亚铁铵晶体)的成分,下列实验操作及叙述中不正确的是( )
| A. | 取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中含有结晶水 | |
| B. | 取少量样品溶于水,向溶液中滴入几滴新制氯水,再滴入2滴KSCN溶液,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 取少量样品溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- | |
| D. | 取少量样品放入试管中,加入少量浓NaOH溶液并加热,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
11. 将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=160mL时,则V2为( )
将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=160mL时,则V2为( )
 将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=160mL时,则V2为( )
将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=160mL时,则V2为( )| A. | 240mL | B. | 300mL | C. | 400mL | D. | 440mL |
10.下列实验操作、实验现象和实验结论不对应的是( )
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近 | 产生大量白烟 | 氨气与氯化氢反应 |
| B | 将洁净铁片放入浓硫酸或浓硝酸中 | 无明显变化 | 常温下,浓硫酸、浓硝酸使铁片钝化 |
| C | 在导管口点燃纯净的氢气,然后将导管伸入盛满氯气的集气瓶中 | 产生苍白色火焰 | 物质燃烧不一定需要氧气 |
| D | 加热试管中的氯化铵固体 | 试管底部的固体逐渐消失 | 氯化铵受热升华 |
| A. | A | B. | B | C. | C | D. | D |
9.下列关于氧化还原反应的叙述中,正确的是( )
| A. | 有单质参加的反应一定是氧化还原反应 | |
| B. | 一种物质被氧化,必有另一种物质被还原 | |
| C. | 2Fe+3Cl2═2FeCl3; Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS 由此可以判断氧化性:Cl2>S | |
| D. | Mg在化学反应中失去2个电子,而Al在化学反应中失去3个电子,因此还原性Al>Mg |
8.在FeCl3溶液中,加入过量的铜粉,充分反应后,溶液中一定不存在的金属离子是( )
0 172023 172031 172037 172041 172047 172049 172053 172059 172061 172067 172073 172077 172079 172083 172089 172091 172097 172101 172103 172107 172109 172113 172115 172117 172118 172119 172121 172122 172123 172125 172127 172131 172133 172137 172139 172143 172149 172151 172157 172161 172163 172167 172173 172179 172181 172187 172191 172193 172199 172203 172209 172217 203614
| A. | Fe2+和Cu2+ | B. | Fe3+ | C. | Cu2+ | D. | Fe2+ |
 、
、